
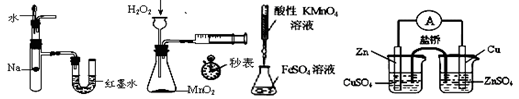
| A.验证反应的热效应 | B.定量测定化学反应速率 |
| C.滴定法测FeSO4 | D.构成铜锌原电池溶液的浓度 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.苯和浓溴水用铁做催化剂制溴苯 |
| B.将苯与浓硝酸混合共热制硝基苯 |
| C.甲烷与氯气光照制得纯净的一氯甲烷 |
| D.乙烯通入溴的四氯化碳溶液得到1,2—二溴乙烷 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
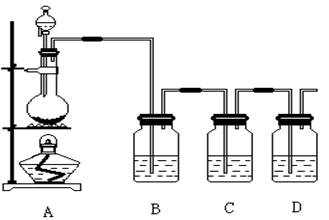
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.配制银氨溶液:在一定量AgNO3溶液,滴加氨水至沉淀恰好溶解。 |
| B.在检验醛基配制Cu(OH)2悬浊液时:在一定量CuSO4溶液中加入少量NaOH溶液 |
| C.验证RX为碘代烷,把RX与烧碱水溶液混合加热将溶液冷却后再加入硝酸银溶液 |
| D.无水乙醇和浓硫酸共热到170℃,将制得的气体通入酸性高锰酸钾,可检验制得的气体是否为乙烯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
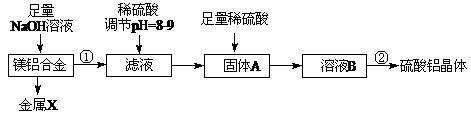
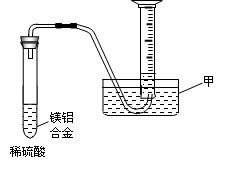
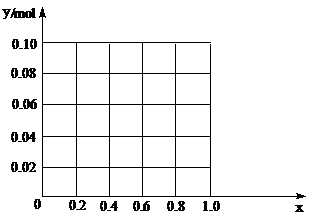
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入溴水,溴水褪色后加热观察能否恢复原色 | 验证SO2漂白的可逆性 |
| B | 将氯水加入淀粉KI溶液中 | 验证Cl的非金属性比I强 |
| C | 把铁块和铜块用导线连接插入浓硝酸中 | 组成原电池验证Fe比Cu活泼 |
| D | 加热氯化铵和碘单质的固体混合物 | 分离除去碘单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
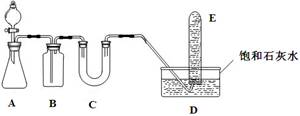
|
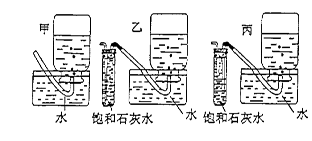
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
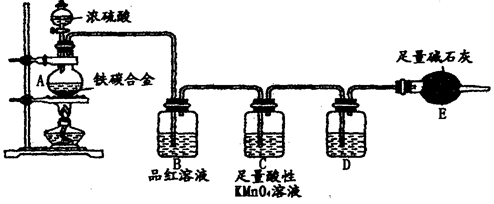

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com