
(1)(广东)由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)===3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) ΔH
①上述反应中,副产物矿渣可用来________。
②已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)===6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) ΔH1
2Ca3(PO4)2(s)+10C(s)===P4(g)+6CaO(s)+10CO(g) ΔH2
SiO2(s)+CaO(s)===CaSiO3(s) ΔH3
用ΔH1、ΔH2和ΔH3表示ΔH,ΔH=____________。
(2)(江苏)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)===Cu2+(aq)+H2(g) ΔH1=+64.39 kJ·mol-1
②2H2O2(l)===2H2O(l)+O2(g) ΔH2=-196.46 kJ·mol-1
③H2(g)+ O2(g)===H2O(l) ΔH3=-285.84 kJ·mol-1
O2(g)===H2O(l) ΔH3=-285.84 kJ·mol-1
在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的热化学方程式为______。
(1)①制玻璃 ②ΔH1+3ΔH2+18ΔH3
(2)Cu(s)+H2O2(l)+2H+(aq)===Cu2+(aq)+2H2O(l) ΔH=-319.68 kJ·mol-1
【解析】 (1)①CaSiO3为玻璃的成分之一,从而确定矿渣用途。②根据盖斯定律知ΔH=ΔH1+3ΔH2+18ΔH3。
(2)由热化学方程式①+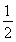 ×②+③得:
×②+③得:
Cu(s)+2H+(aq)+H2O2(l)===Cu2+(aq)+2H2O(l)
ΔH=ΔH1+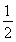 ×ΔH2+ΔH3=+64.39 kJ·mol-1+
×ΔH2+ΔH3=+64.39 kJ·mol-1+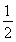 ×(-196.46 kJ·mol-1)+(-285.84 kJ·mol-1)
×(-196.46 kJ·mol-1)+(-285.84 kJ·mol-1)
=-319.68 kJ·mol-1。


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源:2013-2014学年高考化学二轮复习四川配套训练 第12讲化学实验基础练习卷(解析版) 题型:选择题
为提纯下列物质(括号内的物质是杂质)所选用的除杂试剂和分离方法都正确的是( )。
被提纯的物质除杂试剂分离方法
A溴化钠溶液(NaI)新制氯水、CCl4萃取、分液
B氯化铵溶液(FeCl3)氢氧化钠溶液过滤
C二氧化碳(CO)氧化铜粉末通过灼热的氧化铜粉末
D碳酸钠(偏铝酸钠)盐酸过滤
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题8电化学原理练习卷(解析版) 题型:选择题
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示。则下列说法正确的是( )。

A.构成原电池时b极反应为Cu-2e-===Cu2+
B.构成电解池时a极质量一定减少
C.构成电解池时b极质量可能减少也可能增加
D.构成的原电池或电解池工作后可能产生大量气体
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题6化学反应速率和化学平衡练习卷(解析版) 题型:填空题
氨是最重要的化工产品之一。
(1)合成氨用的氢气可以甲烷为原料制得。有关化学反应的能量变化如下图所示。

反应①②③为________反应(填“吸热”或“放热”)。
CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________。
(2)用氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g)。
CO(NH2)2(l)+H2O(g)。
①某温度下,向容积为10 L的密闭容器中通入2 mol NH3和1 mol CO2,反应达到平衡时CO2的转化率为50%。该反应的化学平衡常数表达式为K=______。该温度下平衡常数K的计算结果为_____。
②为进一步提高CO2的平衡转化率,下列措施中能达到目的的是________。
A.提高NH3的浓度 B.增大压强
C.及时转移生成的尿素 D.使用更高效的催化剂
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题6化学反应速率和化学平衡练习卷(解析版) 题型:选择题
下列条件一定能使反应速率加快的是( )。
①增加反应物的物质的量 ②升高温度 ③增大反应体系的压强 ④不断分离出生成物 ⑤加入MnO2
A.全部 B.①②⑤ C.② D.②③
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题5化学反应与能量变化练习卷(解析版) 题型:选择题
工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为放热反应。现将2 mol SO2、1 mol O2充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO2的转化率为50%。下列热化学方程式正确的是( )。
A.2SO3(g) 2SO2(g)+O2(g) ΔH=+196.6 kJ·mol-1
2SO2(g)+O2(g) ΔH=+196.6 kJ·mol-1
B.2SO2(g)+O2(g) SO3(g) ΔH=-98.3 kJ·mol-1
SO3(g) ΔH=-98.3 kJ·mol-1
C.SO2(g)+ O2(g)
O2(g) SO3(g) ΔH=+98.3 kJ·mol-1
SO3(g) ΔH=+98.3 kJ·mol-1
D.SO2(g)+ O2(g)
O2(g) SO3(g) ΔH=-196.6 kJ·mol-1
SO3(g) ΔH=-196.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题4物质结构与元素周期律练习卷(解析版) 题型:填空题
下表列出了A~R十种元素在周期表中的位置:
主族
周期 ⅠAⅡAⅢAⅣAⅤAⅥAⅦA
2ERF
3ACDHIG
4B
请回答下列问题:
(1)写出R单质分子的电子式________。
(2)A、C、D三种元素的最高价氧化物对应的水化物中碱性最强的是________(填化学式)。
(3)A、B、C三种元素的阳离子按离子半径由大到小的顺序排列为________(用元素的离子符号表示)。
(4)写出A的单质与水反应的化学方程式_____________________________。
(5)X元素是A~R十种元素中的一种,X的原子核里有14个中子,2.7 g X在氧气里燃烧时,质量增加2.4 g。X的氢氧化物既能与氢氧化钠溶液反应,也能与盐酸反应。X的元素符号是________,它位于元素周期表中第________周期第________族。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题3中学化学常见的两种重要反应类型练习卷(解析版) 题型:选择题
下表所列各组第Ⅰ栏中的化学反应与第Ⅱ栏中的化学反应,都可以用第Ⅲ栏中的离子方程式表示的是( )。
选项第Ⅰ栏第Ⅱ栏第Ⅲ栏
A往少量NaOH溶液中投入铝片往过量NaOH溶液中投入铝片2Al+2OH-+
2H2O===2AlO2—
+3H2↑
B往Fe2(SO4)3溶液中滴入NaOH溶液往Fe2(SO4)3溶液中滴入Ba(OH)2溶液 Fe3++3OH-===Fe(OH)3↓
C往NaHCO3溶液中滴入Ca(OH)2溶液往NaHCO3溶液中滴入NaOH溶液 OH-+HCO3—====CO32—+H2O
D往NaOH溶液中通入过量CO2气体往NaOH溶液中通入少量CO2气体CO2+OH-===HCO3—
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题1物质的组成分类性质及化学用语练习卷(解析版) 题型:选择题
下列化学用语使用不正确的是( )。
A.Na+的结构示意图为
B.明矾的化学式为KAl(SO4)2·12H2O
C.聚乙烯的结构简式为CH2===CH2
D.高氯酸(HClO4)中氯元素的化合价为+7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com