
| �¶� / �� | 25 | t1 | t2 |
| ˮ�����ӻ����� | 1��10��14 | �� | 1��10��12 |
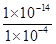 ��1��10��10mol/L����ˮϡ��1000������������Խ��ͣ����������Լ��ԣ�������ϡ�ͺ���Һ��pH��7��
��1��10��10mol/L����ˮϡ��1000������������Խ��ͣ����������Լ��ԣ�������ϡ�ͺ���Һ��pH��7��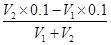 ��0.01����V1��V2��9:11��
��0.01����V1��V2��9:11��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0.01mol/L CH3COOH | B��0.01mol/L HNO3 |
| C��pH��2��H2SO4��Һ | D��pH��2��CH3COOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��11��1 | B��9��1 | C��1��11 | D��1��9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 H++OH�����ƣ�����Һ�����Ե���
H++OH�����ƣ�����Һ�����Ե���| A����ˮ�м����������������� |
| B����ˮ�м��������������ƹ��� |
| C����ˮ�м�������̼���ƹ��� |
| D����ˮ���ȵ�100�棬ʹˮ��pH=6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��1��9 | B��9��1 | C��1��11 | D��11��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��c(H+)��c(Cl-)��c(OH-) |
| B��c(H+)��c(OH-)��1.0��10��14 |
| C����ˮ�������c(H+)��1.0��10��13mol?L-1 |
| D����pH��13��NaOH��Һ��Ϻ����Һһ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
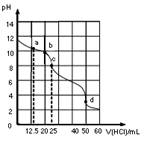
| A��a�㣺c��CO32-��=c(HCO3-)>c(OH-) |
| B��b�㣺5c(Cl-)>4c(HCO3-)+4c(CO32-) |
| C��c�㣺c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| D��d�㣺c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaHCO3��Һ�У�c(H+) + c(Na+)��c(HCO3��)+2c(CO32��) + c(OH��) |
| B��pH=12��Ba(OH)2��Һ��pH=12��Na2CO3��Һ�У�ˮ�����c(H��)һ���� |
| C��0.2mol��L��1 HCl��Һ������0.05 mol��L��1 Ba(OH)2��Һ��Ϻ���Һ��pH��1 |
| D����10 mL 0.10mol?L��1CH3COOH��Һ��������ʵ�����NaOH����Һ�����ӵ�Ũ���ɴ�С��˳���ǣ�c(Na+)��c(CH3COO��)��c(OH������c(H+) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ��
�� ��
�� ��NaOH ��
��NaOH �� ��
�� ��
�� ��
�� �����и���������ȷ����
�����и���������ȷ����| A��pH:��>��>��>�� | B�� ����>��>��>�� ����>��>��>�� |
| C����Һ��c(H��): ��>��>��>�� | D�� : ��>��>��>�� : ��>��>��>�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com