
【题目】下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是
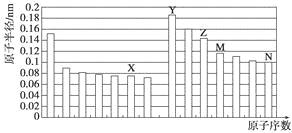
A. Z、N两种元素的离子半径相比,前者较大
B. X、N两种元素的气态氢化物的沸点相比,前者较低
C. 由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D. Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液
【答案】D
【解析】试题分析:同周期从左到右原子半径减小,同主族元素从上而下原子半径增大,故前7种元素处于第二周期,后7中元素处于第三周期,由原子序数可知,X为氧元素,Y为钠元素,Z为铝元素,M为硅元素,N为硫元素,N为氯元素。A、Z、N两种元素的离子分别为钠离子和氯离子,最外层电子数相同,电子层越多离子半径越大,故离子半径钠离子小于氯离子,A错误;B、非金属性氧大于氯,非金属性越强氢化物越稳定,故稳定性水大于氯化氢,B错误;C、由X与M两种元素组成的化合物是二氧化硅,能与氢氟酸反应,C错误;D、氧化铝是良性氧化物,能与氢氧化钠反应生成偏铝算钠,能与盐酸反应生成氯化铝,D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数(NA)的说法错误的是( )
A. 32g O2所含的原子数目为NA
B. 0.5mol H2O含有的原子数目为1.5NA
C. 1mol H2O含有的H2O分子数目为NA
D. 0.5NA个氯气分子的物质的量是0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大.请回答下列问题:
(1)X的原子结构示意图为;Y的价电子轨道表示式为 .
(2)XZ2与YZ2分子的立体结构分别是和 , 相同条件下两者在水中的溶解度较大的是(写分子式),理由是 .
(3)Q的元素符号是 , 它属于第周期族,它的核外电子排布式为 , 在形成化合物时它的最高化合价为
(4)用氢键表示式写出E的氢化物水溶液中存在的所有氢键 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是(NA为阿伏加德罗常数的值) ( )
A. 硫酸的摩尔质量是98 g
B. 1molO2的质量是32g/mol
C. 2g氢气所含原子数目为2NA
D. 标准状况下,11.2LCH4的物质的量为0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等量镁铝合金粉末分别与下列4种过量的溶液充分反应,放出氢气最多的是( )
A.2 mol·L-1 H2SO4溶液
B.18 mol·L-1 H2SO4溶液
C.6 mol·L-1 KOH溶液
D.3 mol·L-1 HNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为短周期主族元素,其原子序数依次增大。其中A元素原子核内只有一个质子;A与C、B与D分别同主族;B、D两元素原子序数之和是A、C两元素原子序数之和的2倍。
请回答下列问题:
(1)由上述元素组成的下列物质中属于非电解质的是________(填字母)。
A.C2B2 B.DB2 C.E2 D.C2DB3
(2)D元素在元素周期表中的位置为_______________________________;化合物C2B中两种离子的半径大小关系为________>________(填离子符号)。
(3)实验室中欲选用下列装置制取并收集纯净干燥的E2气体。实验中应选用的装置为________________(按由左到右的连接顺序填写);
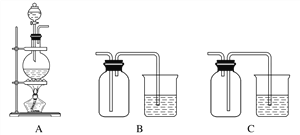
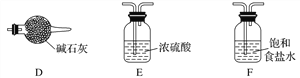
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知4NH3+5O2═4NO+6H2O,同一反应速率若分别用v(NH3)、v(O2)、v(H2O)、v(NO)(molL﹣1min﹣1)来表示,则正确关系是( )
A.![]() v(NH3)=v(O2)
v(NH3)=v(O2)
B.![]() v(O2)=v(H2O)??
v(O2)=v(H2O)??
C.![]() v(NH3)=v(H2O)
v(NH3)=v(H2O)
D.![]() v(O2)=v(NO)
v(O2)=v(NO)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com