
| ||


科目:高中化学 来源: 题型:
| n(CH3OH) |
| n(CO2) |
| A、加入催化剂 |
| B、充入He(g),使体系压强增大 |
| C、将H2O(g)从体系中分离 |
| D、降低温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 在体积为VL的恒容密闭容器中盛有一定量的H2,通往Br2(g)发生反应:H2(g)+Br2(g)?2HBr(g)△H<0.平衡时H2的体积分数与所加入Br2(g)的物质的量变化关系如图所示,下列说法正确的是( )
在体积为VL的恒容密闭容器中盛有一定量的H2,通往Br2(g)发生反应:H2(g)+Br2(g)?2HBr(g)△H<0.平衡时H2的体积分数与所加入Br2(g)的物质的量变化关系如图所示,下列说法正确的是( )| A、由图可知:T1<T2 |
| B、a,b两点的反应速率:a>b |
| C、为了提高Br2的转化率,可采取将HBr及时移走 |
| D、T1时,随着Br2加入,平衡时Br2的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
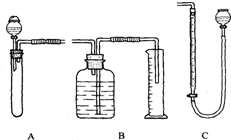 某样品为Na2CO3和NaHCO3固体混合物,现将一定质量的样品与稀盐酸反应,用测定生成CO2体积的方法计算出样品中各组分的质量分数.为较准确地测出生成CO2的体积,在反应结束后加热反应混合物,使溶于溶液中的CO2逸出,待冷却至室温后测CO2的体积(加热时蒸发的水的体积忽略不计).如图是实验装置图,其中,B和C可供选择.请回答下列问题:
某样品为Na2CO3和NaHCO3固体混合物,现将一定质量的样品与稀盐酸反应,用测定生成CO2体积的方法计算出样品中各组分的质量分数.为较准确地测出生成CO2的体积,在反应结束后加热反应混合物,使溶于溶液中的CO2逸出,待冷却至室温后测CO2的体积(加热时蒸发的水的体积忽略不计).如图是实验装置图,其中,B和C可供选择.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、脱脂棉的主要成分是纤维素,人造丝和蚕丝的主要成分都是蛋白质 |
| B、淀粉、油脂、蛋白质都是高分子化合物,在一定条件下都能发生水解 |
| C、肽链通过氢键按一定的规律卷曲或折叠形成的空间结构称为蛋白质的二级结构 |
| D、淀粉与稀硫酸混合加热后,加入新制氢氧化铜加热,可检验淀粉是否已水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C(SO42-)>C(NH4+)>C(OH-)>C(H+) |
| B、C(NH4+)>C(SO42-)>C(H+)>C(OH-) |
| C、C(SO42-)>C(NH4+)>C(H+)>C(OH-) |
| D、C(SO42-)>C(H+)>C(NH4+)>C(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com