
科目:高中化学 来源: 题型:



查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
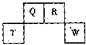 (2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(2012?长宁区一模)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年甘肃省武威第五中学高一3月月考化学试卷(带解析) 题型:填空题
(12)某元素R原子的核外电子数等于核内中子数,该元素的单质2.8g与氧气充分反应,生成6.0g的化合物RO2。请回答:
(1)元素R的原子序数是 。
(2)元素R的原子共有 个电子层,能量最低的电子层中共有 个电子。
(3)写出元素R的最高价氧化物对应水化物的化学式 ,它的酸性比碳酸的酸性 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年山西省高三下学期模拟考试(理综)化学部分 题型:填空题
(15分)下表是元素周期表的一部分,用元素符号或化学式回答下列问题:
|
主族周期 |
IA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
1 |
|
|
|
|
|
|
|
① |
|
2 |
|
|
|
|
② |
③ |
④ |
|
|
3 |
⑤ |
⑥ |
⑦ |
|
⑧ |
⑨ |
⑩ |
|
(1)在这些元素中_______是最活泼的金属元素;其氢氧化物具有两性的元素是
(2)这些元素的最高价氧化物对应的水化物中酸性最强的物质的化学式_________
(3)从⑤到⑩元素中_______原子半径最小。
(4)最不活泼的元素的单质的化学式是 。若该元素某核素原子核内中子数与质子数相等,则该核素的摩尔质量是
(5)用电子式表示⑩、⑥两元素形成化合物的过程
(6)与元素⑨非金属性强弱最接近的元素是
(7)根据下表判断:最接近磷原子半径R(10-10m)的取值范围的是
|
元 素 |
N |
S |
O |
Si |
|
原子半径/10-10m |
0.75 |
1.02 |
0.74 |
1.17 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com