
| A. | 玻璃棒 | B. | 容量瓶 | C. | 漏斗 | D. | 胶头滴管 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所得溶液中氯化钠的浓度为1 mol/L | |
| B. | 向所得的溶液中通入二氧化碳,可使溶液具备漂白性 | |
| C. | 所得溶液中有大量的单质的氯元素存在 | |
| D. | 在反应中氯元素化合价降低,钠元素化合价升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,通过用pH试纸测定浓度为0.1 mol•L-1 NaClO溶液和0.1 mol•L-1 CH3COONa溶液的pH来比较HClO和CH3COOH的酸性强弱 | |
| B. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| C. | 用高锰酸钾溶液滴定Na2SO3溶液至终点:滴入最后一滴高锰酸钾溶液,溶液恰好由紫色变为无色,半分钟不变色 | |
| D. | 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,用NaOH溶液滴定20.00mL0.1mol•L-1CH3COOH溶液所得滴定曲线如图,下列说法正确的是( )
常温下,用NaOH溶液滴定20.00mL0.1mol•L-1CH3COOH溶液所得滴定曲线如图,下列说法正确的是( )| A. | 点①所示溶液中:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+) | |
| B. | 点②所示溶液中:c(Na+)═c(CH3COOH)+c(CH3COO-) | |
| C. | 点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定过程中不可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
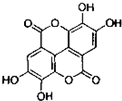 ).
).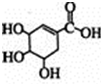 +Br2→
+Br2→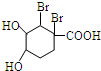 .
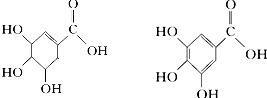
.
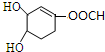 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
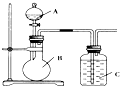 某同学设计如图装置,研究非金属元素性质变化规律.
某同学设计如图装置,研究非金属元素性质变化规律.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3(CH2)15SO3Na | B. | 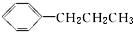 | C. | CCl4 | D. | CH3(CH2)4COOCH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com