
| A.Al2S3 | B.Fe2S3 | C.FeCl3 | D.CuS |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 |
| A.2SO2+O22SO3 | B.SO2+H2O H2SO3 H2SO3 |
| C.SO2+2H2S====3S↓+2H2O | D.SO2+Cl2+2H2O====H2SO4+2HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
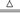 2Fe2O3+8SO2
2Fe2O3+8SO2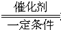 2SO3
2SO3 H2SO4
H2SO4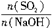 =x,试写出x在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)间的关系式。
=x,试写出x在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)间的关系式。| x=n(SO2)/n(NaOH) | n(NaHSO3) |
| | |
| | |
| | |
 Na2SO3+H2O;NaOH+SO2
Na2SO3+H2O;NaOH+SO2  aHSO3。根据题给条件,对上述反应运用极值假设法进行分析讨论。第(3)步考查计算题中范围讨论的基础知识,以及过量问题和平行反应的计算。
aHSO3。根据题给条件,对上述反应运用极值假设法进行分析讨论。第(3)步考查计算题中范围讨论的基础知识,以及过量问题和平行反应的计算。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②④ | B.②⑤⑥ |
| C.①②④⑤ | D.②④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.10mL 18.4mol/L H2SO4 | B.30mL 3mol/L盐酸 |
| C.30mL 2mol/L H2SO4 | D.30mL 5mol/L HNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com