
分析 ①石油的分馏实验中温度计测量馏分温度;
②氢氧化铜浊液应该呈碱性;
③苯酚易溶于酒精;
④配制银氨溶液:在一定量AgNO3溶液中滴加氨水,使生成的沉淀恰好溶解即可;
⑤苯酚和溴都易溶于苯;
⑥卤代烃中卤元素检验需要酸性条件下.
解答 解:①石油的分馏实验中温度计测量馏分温度,所以温度计水银球应该位于蒸馏烧瓶支管口处,故错误;
②氢氧化铜浊液应该呈碱性,NaOH应该过量,该混合溶液中硫酸铜过量而导致溶液呈酸性,故错误;
③苯酚易溶于酒精,所以不慎将苯酚溶液沾到皮肤上,立即用酒精清洗,故正确;
④配制银氨溶液:在一定量AgNO3溶液中滴加氨水,使生成的沉淀恰好溶解即可,故错误;
⑤苯酚和溴都易溶于苯,应该用NaOH溶液除去苯酚,然后用分液方法分离,故错误;
⑥卤代烃中卤元素检验需要酸性条件下,所以水解后应该加硝酸中和剩余的碱,故错误;
故答案为:③.
点评 本题考查化学实验方案评价,为高频考点,侧重考查基本操作及物质性质,明确实验原理及操作规范性是解本题关键,注意某些反应对溶液酸碱性的要求,题目难度不大.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 该技术可用于观察一些胶体粒子的运动 | |
| B. | 该技术可用于观察一些大分子蛋白质的合成 | |
| C. | 该技术使观察水的分子团簇结构成为可能 | |
| D. | 该技术可用于分辨荧光分子中各种不同种类的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2--无色气体 | B. | BaSO4--灰绿色固体 | ||
| C. | Al(OH)3--白色固体 | D. | H2O--白色液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应属于置换反应 | |
| B. | 该反应中氧化剂为I2 | |
| C. | 该反应中还原剂为KClO3 | |
| D. | 该反应中KClO3被还原为Cl2,I2被氧化为KIO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 6种相邻短周期主族元素的相对位置如表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
6种相邻短周期主族元素的相对位置如表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:| X | Y | Z | |
| W | M | Q |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
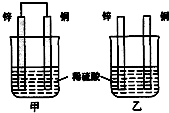 (1)已知:△H>0为吸热反应、△H<0为放热反应.实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C.
(1)已知:△H>0为吸热反应、△H<0为放热反应.实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 头孢羟氨苄(如图)被人体吸收效果良好,疗效明显,且毒性反应较小,因而被广泛适用于敏感细菌所致的多种疾病治疗.下列对头孢羟氨苄的说法中正确的是( )
头孢羟氨苄(如图)被人体吸收效果良好,疗效明显,且毒性反应较小,因而被广泛适用于敏感细菌所致的多种疾病治疗.下列对头孢羟氨苄的说法中正确的是( )| A. | 头孢羟氨苄可与NaOH溶液反应但不与HCl反应 | |
| B. | 该化合物中含有4个手性碳原子 | |
| C. | 在催化剂存在条件下,1mol头孢羟氨苄可与7molH2发生反应 | |
| D. | 头孢羟氨苄不能在空气中稳定存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com