
| A. | 工业生产硫酸的过程中使用过量的空气,以提高二氧化硫的转化率 | |
| B. | 氯化镁溶液加热蒸干最终得不到氯化镁固体 | |
| C. | 合成氨是放热反应,采用在较高温度下进行反应 | |
| D. | 实验室用排饱和食盐水的方法收集氯气 |
分析 勒沙特列原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动.勒沙特列原理适用的对象应存在可逆过程,如与可逆过程无关,则不能用勒沙特列原理解释.
解答 解:A.增大空气的量,即增大反应物浓度,平衡正向移动,所以可以提高二氧化硫的转化率,能用勒夏特列原理解释,故A不选;
B.氯化镁水解生成HCl和氢氧化镁,升高温度促进盐酸挥发,从而促进氯化镁水解,所以可以用勒夏特列原理解释,故B不选;
C.合成氨是放热反应,升高温度,平衡逆向移动,所以不能采用较高温度,不能用勒夏特列原理解释,故C选;
D.氯气和水反应生成HCl、HClO,NaCl电离出的氯离子抑制氯气和水反应,所以可以用排饱和食盐水的方法收集氯气,可以用勒夏特列原理解释,故D不选;
故选C.
点评 本题考查勒夏特列原理,为高频考点,明确勒夏特列原理含义是解本题关键,注意勒夏特列原理适用范围,只有改变条件时能引起平衡移动的才能用勒夏特列原理解释,题目难度不大.


 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:多选题
| A. | H-H键无方向性 | |
| B. | 基态C原子有两个未成对电子,所以最多只能形成2个共价键 | |
| C. | 1个N原子最多只能与3个H原子结合形成NH3分子,是由共价键的饱和性所决定的 | |
| D. | 气体单质中,一定有σ键,可能有π键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应物分子必须碰撞才有可能发生反应 | |
| B. | 反应速率大小与单位时间内反应物分子间的碰撞次数成正比 | |
| C. | 有效碰撞是活化分子在一定方向上的碰撞 | |
| D. | 活化分子的平均能量称为活化能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的稳定性:D>C | B. | 原子半径:B>A>C>D | ||
| C. | 单质的还原性:B>A | D. | 原子序数:b>a>c>d |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ⑤③④①② | C. | ③④⑤②① | D. | ⑤②①④③ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
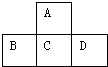 图是周期表的一部分,已知A、B、C、D都是短周期元素,四种元素原子核外共有56个电子,推断A、B、C、D各是什么元素,写出他们的元素符号:AO,BP,CS,DCl.
图是周期表的一部分,已知A、B、C、D都是短周期元素,四种元素原子核外共有56个电子,推断A、B、C、D各是什么元素,写出他们的元素符号:AO,BP,CS,DCl.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,0.1mol/L的KOH溶液和0.1mol/L的醋酸溶液中,由水电离的OH-浓度 | |
| B. | 常温常压下,0.1mol/L的KOH溶液和0.1mol/L的盐酸溶液中,由水电离的OH-浓度 | |
| C. | 25℃,100mL0.1mol/L醋酸溶液与10 mL 1 mol/L醋酸溶液中的k(HAc) | |
| D. | 100mL0.1mol/L醋酸溶液与10 mL 1 mol/L醋酸溶液中H+的数目 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com