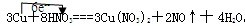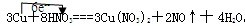已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu+8HNO3══3Cu(NO3)2+2NO↑+4H2O
(1)用单线桥法分析上述反应.
(2)上述反应的离子方程式为______,还原产物是______(填化学式). 标况下生成3.36L NO,被还原的硝酸的物质的量为______.
解:(1)化合价升高元素Cu失电子,化合价降低元素N得到电子,化合价升高数=化合价降低数=转移电子数=6,电子转移情况如下:
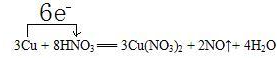
,故答案为:
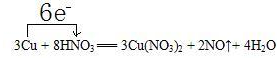
;
(2)铜和硝酸反应的离子方程式为:3Cu+8H
++2NO
3-══3Cu
2++2NO↑+4H
2O,化合价降低元素的N元素所在的反应物HNO
3是氧化剂,对应的产物NO是还原产物,在参加反应的8mool硝酸中,被还原的硝酸的物质的量为2mol,生成NO的物质的量是2mol,当生成标况下3.36L即0.15molNO时,参加反应的硝酸的物质的量为0.6mol,其中被还原的硝酸的物质的量为0.15ml,故答案为:3Cu+8H
++2NO
3-══3Cu
2++2NO↑+4H
2O;NO;0.15mol.
分析:(1)化合价升高元素失电子,化合价降低元素得到电子,化合价升高数=化合价降低数=转移电子数;
(2)根据离子方程式的书写方法来书写离子方程式,在氧化还原反应中,化合价降低元素所在的反应物是氧化剂,对应产物是还原产物,化合价升高元素所在的反应物是还原剂,对应产物是氧化产物,根据硝酸的作用以及方程式进行计算.
点评:本题考查学生氧化还原反应的有关知识,可以根据所学知识进行回答,难度不大.

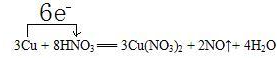 ,故答案为:
,故答案为: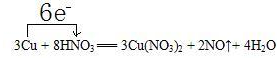 ;
;