
【题目】漂白粉的有效成分是( )
A.Ca(OH)2
B.Ca(ClO)2
C.CaCl2
D.CaCO3
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】氨是重要的工业原料,在农业、医药、国防和化工等领域有重要应用。
I.(1)工业上用N2和H2在一定条件下合成氨,下列措施能使正反应速率增大,且使平衡混合物中NH3的体积分数一定增大的是________。
A.降低反应温度 B.压缩反应混合物 C.充入N2 D.液化分离NH3
(2)常温下向100mL0.2mo/L的氨水中逐滴加入0.2mol/L的盐酸,所得溶液的pH、溶液中NH4+和NH3·H2O物质的量分数与加入盐酸的体积的关系如下图所示,根据图像回答下列问题。

①表示NH3·H2O浓度变化的曲线是__________(填“A”或“B")。
②NH3·H2O的电离常数为_______(已知lg1.8 = 0.26)。
③当加入盐酸体积为50ml时,溶被中c(NH4+)- c(NH3·H2O) =_____mol/L (用数字表示)。
Ⅱ.若液氨中也存在类似水的电离( H2O+H2O![]() H3O+ +OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
H3O+ +OH-),碳酸钠溶于液氨后也能发生完全电离和类似水解的氨解。
(1)写出液氨的电离方程式_________.
(2)写出碳酸钠溶于液氨后第一级氨解的离子方程式__________
(3)写出碳酸钠的液氨溶液中各离子浓度的大小关系____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的某溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如下:

下列有关推断不正确的是
A. 沉淀H为AI(OH)3、BaCO3的混合物
B. 根据上述连续实验不能确定溶液X中是否含有Fe3+、Cl-
C. 溶液X中一定含有Al3+、NH4+、Fe2+、SO42-、H+
D. 若溶液X为100mL,产生的气体A为44.8mL(标况),则X中c(Fe2+)=0.06mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2020年春节期间举行的《中国诗词大会》第五季精彩纷呈,体现了中国诗词博大精深,下列诗词分析错误的是
A.“弄风柳絮疑成雪,满地榆钱买得春”中的“柳絮”和棉花的成分均含纤维素
B.“日暮汉宫传蜡烛,轻烟散入五侯家”中的“蜡烛”是高级脂肪酸酯,也是高分子化合物
C.“炎炎日正午,灼灼火俱燃”中的“炎炎”体现自然界中太阳能与热能的转化
D.“煮豆持作羹,漉鼓以为汁”中的“漉鼓”涉及的基本操作是过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示。下列说法中,正确的是

A. 图中A、D、E三点处KW间的关系:E处>A处>D处
B. 温度不变时,往水中通入适量HCl气体,可以使水的电离从A点变化到D点
C. 温度不变时,在水中加入适量CH3COONa固体,可以使水的电离从A点变化到C点
D. 在B点处,0.5 mol·L-1的H2SO4溶液与1 mol·L-1的KOH溶液等体积混合,充分反应后,所得溶液的pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是常见的有机物质,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平.有关物质的转化关系如图1所示,请回答下列问题: 
(1)B的结构式为 . D的物质的名称是 .
(2)在①~④反应中,属于加成反应的是(填反应序号).
(3)写出下列反应的化学方程式:
反应①;反应②;反应③ .
(4)实验室用如图2所示装置进行反应④.
a.反应④的化学方程式是 .
b.试管乙中应加入,乙中的导管不能伸入到液面下的原因是 .
c.实验完成后,从试管乙中分离出有机物C的方法是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体。某研究小组用下图所示的实验装置,利用浓氨水、干冰等作原料制备氨基甲酸铵。
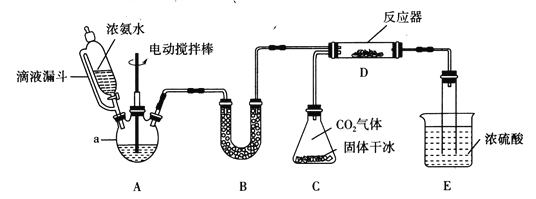
(1)仪器a的名称是____________;与分液漏斗相比,使用滴液漏斗的优点是:______________________________________。
(2)装置B中盛装药品的名称是________________。
(3)写出装置D中发生反应的化学方程式:__________________________________。
(4)装置E的作用之一是控制原料气按反应计量系数充分反应。若反应初期观察到装置内浓硫酸中产生气泡,应该______(填“加快”、“减慢”或“不改变”)产生氨气的流速;装置E的作用还有___________________________________________________。
(5)已知氨基甲酸铵可完全水解为碳酸氢铵。为测定氨基甲酸铵样品的纯度,取样品1.600g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为2.000g。
①写出碳酸氢铵与足量石灰水反应的离子方程式:______________________________。
②样品中氨基甲酸铵的质量分数为_____________%。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.2L标准状况下的甲烷和某单烯羟的混合气体通入足量的溴的四氯化碳溶液中充分反应,溴的四氯化碳溶液增加了12.6g.该烯羟对氢气的相对密度为21(相对密度 ![]() )
)
①试确定该烯烃;
②求原混合气体中甲烷与烯烃的物质的量之比以及质量之比.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com