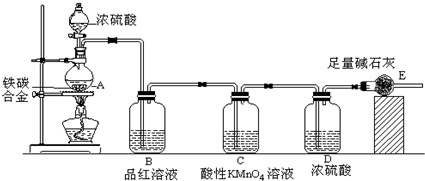
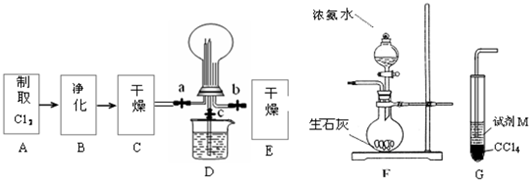
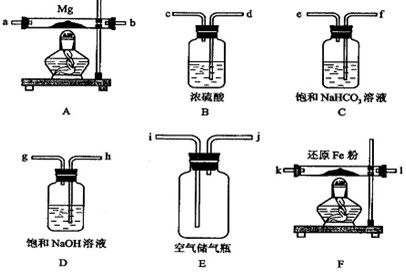
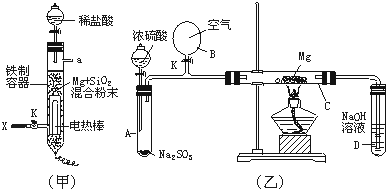
(2013?浦东新区三模)某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹).
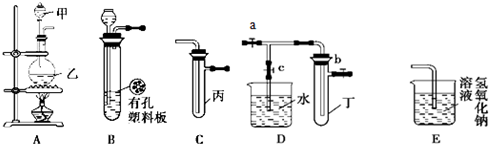
请按要求填空:?
(1)利用B装置可制取的气体有
H2、CO2、H2S等
H2、CO2、H2S等
(填2种).
(2)A、C、E相连后的装置可用于制取Cl
2并进行相关的性质实验.
若在丙中加入适量水,即可制得氯水.将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如下:?
| 实验序号 |
实验操作 |
现象 |
结论 |
| Ⅰ |
将氯水滴入品红溶液 |
溶液褪色 |
氯气与水反应的产物有漂白性 |
| Ⅱ |
氯水中加入 NaHCO3粉末 |
有无色气泡产生 |
氯气与水反应的产物具有较强的酸性 |
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理,请说明理由.
不合理,没有事先证明干燥的氯气无漂白性;不合理;制取的氯气中含有HCl气体,HCl溶于水后能与碳酸氢钠粉末反应产生气泡
不合理,没有事先证明干燥的氯气无漂白性;不合理;制取的氯气中含有HCl气体,HCl溶于水后能与碳酸氢钠粉末反应产生气泡
.
(3)请利用上述A、C装置设计一个简单的实验,验证Cl
2和Br
2的氧化性强弱(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)
在甲、乙、丙中分别装入浓盐酸、二氧化锰、溴化钠溶液;烧瓶中有黄绿色气体生成,试管中溶液由无色变为橙色,可证明氯气的氧化性强于溴
在甲、乙、丙中分别装入浓盐酸、二氧化锰、溴化钠溶液;烧瓶中有黄绿色气体生成,试管中溶液由无色变为橙色,可证明氯气的氧化性强于溴
.B、D、E装置相连后,在B中盛装足量浓硝酸和铜片(放在有孔塑料板上),可制得NO
2并进行有关实验.
(4)B中发生反应的化学方程式为
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
.
(5)欲用D装置验证NO
2与水的反应,其操作步骤为:先关闭止水夹
a、b
a、b
,再打开止水夹
c
c
,使烧杯中的水进入试管丁的操作是
双手紧握(或微热)试管丁使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流入试管丁
双手紧握(或微热)试管丁使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流入试管丁
.
(6)试管丁中的NO
2与一定量的O
2混合后倒插水中,试管9/10充满水,则原试管丁中的混合气体的平均分子量可能为
42.08或44.04
42.08或44.04
.(保留二位小数)



 阅读快车系列答案
阅读快车系列答案