
【题目】手持技术的氧电化学传感器可用于测定 O2含量,右图为某种氧电化学传感器的 原理示意图。已知在测定O2含量过程 中,电解质溶液的质量保持不变。一定时 间内,若通过传感器的待测气体为aL(标 准状况),某电极增重了b g。下列说法正确的是
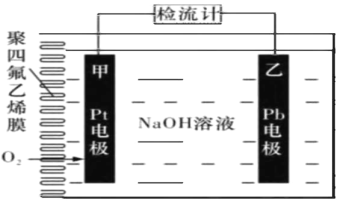
A.Pt电极为负极
B.反应过程中转移OH-的物质的量为0.125bmol
C.Pb电极上发生的电极反应为Pb-2e- +2OH- = Pb(OH)2
D.待测气体屮氧气的体积分数为![]()
【答案】B
【解析】
A. 得电子发生还原反应的电极是正极、失电子发生氧化反应的电极是负极,则通入氧气的电极Pt电极为正极,发生还原反应,故A错误;
B. 放电过程中,Pb电极质量增加,增加的质量为氧元素质量,如果电极质量增加bg,则生成n(PbO)=n(O)=![]() mol,根据2Pb+4OH4e═2PbO+2H2O得转移n(OH)=2n(PbO)
mol,根据2Pb+4OH4e═2PbO+2H2O得转移n(OH)=2n(PbO)
=0.125bmol,故B正确;
C. 在测定O2含量过程中,电解质溶液的质量保持不变,说明Pt电极消耗的氧气与Pb电极上得到的O原子质量相等,其电池反应式为2Pb+O2=2PbO,所以Pb电极上Pb失电子和OH反应生成PbO,电极反应式为2Pb+4OH4e═2PbO+2H2O,故B错误;
D. 根据转移电子相等得:n(O2)=![]() n(PbO)=
n(PbO)= ![]() bmol,氧气体积=
bmol,氧气体积=![]() bmol×22.4L/mol=0.7bL,待测氧气体积分数=
bmol×22.4L/mol=0.7bL,待测氧气体积分数=![]() ,故D错误;
,故D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=____,ΔH=___(填“<”、“>”或“=”)0。
(2)830℃时,向一个5 L的密闭容器中充入0.20molA和0.80molB,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6 s时c(A)=____mol·L-1,C的物质的量为___mol;若反应经一段时间后,达到平衡时A的转化率为____,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为_____。
(3)判断该反应是否达到平衡的依据为_____。
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 强电解质溶液的导电能力一定比弱电解质溶液的强
B. 一定温度下,可逆反应2X(g)+Y(g)![]() 2Z(g)达到平衡的标志是:容器内X、Y、Z的物质的量之比为2:1:2
2Z(g)达到平衡的标志是:容器内X、Y、Z的物质的量之比为2:1:2
C. 升高温度,AgCl的溶解度增大,Ksp增大
D. FeCl3、KAl(SO4)2、Na2CO3的水溶液均显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制流程:

依照上述流程回答以下问题:
(1)混合①中发生反应的化学方程式为_______。
(2)操作Ⅱ和操作Ⅲ的名称分别是_______、_______。操作Ⅲ一般适用于分离____________混合物。〔选填编号〕
a、固体和液体b、固体和固体c、互不相溶的液体d、互溶的液体
(3)混合②中加入Na2SO3的目的是_______。
(4)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸〔工业氢溴酸〕带有淡淡的黄色。因此甲乙两同学设计了简单实验加以探究:甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,那么用于证明该假设所用的试剂的名称为_______。乙同学假设工业氢溴酸呈淡黄色是因为________,其用于证明该假设所用的试剂的化学式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示有关物质的相互转化关系,其中A是由G和某淡黄色固体组成的混合物,I是常见的无色液体,反应①在化工生产中有着重要应用(部分产物和条件已略去)。

(1)写出以下物质的化学式:B_______、F_______。
(2)反应②的离子方程式为_______。
(3)我国首创的由G、空气和海水组成的电池,在航海领域有着极其重要的作用,其工作时正极反应式为_______,该电池最大的优点是只需补充_______〔填“正极”或“负极”〕材料就可接着使用。
(4)向M的水溶液中加入少量A中的淡黄色固体,反应的化学方程式为_______。
(5)25℃时,pH均为5的盐酸和M的水溶液中,由H2O电离出的H+物质的量浓度之比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学家利用二氧化饰(CeO2)在太阳能作用下将H2O、CO2转变为H2、 CO,其过程如下所示:
mCeO2![]() (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+x H2O+xCO2![]() mCeO2+xH2+xCO2
mCeO2+xH2+xCO2
下列说法不正确的是
A.该过程中CeO2是H2O、CO2转变为H2、CO反应的催化剂
B.利用CeO2作催化剂-既可使该转变过程速率提高。亦可减小能量的消 耗,并可提高反应物转化率
C.mmol CeO2参加反应,气体物质的量增加x mol
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH - - 2e = CO32- +2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如图所示的转化关系。根据图示转化关系推测下列说法正确的是
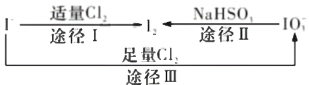
A.可用淀粉-KI试纸和食醋检验加碘盐中是否含有碘元素
B.向淀粉-KI溶液中通入过量Cl2,最终溶液呈蓝色
C.由图可知氧化性的强弱顺序为C12 >I2 >IO3-
D.途径1和II中各自生成1 mol I2,反应中转移的电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷((POCl3)可用于制备增塑剂,常温下为无色透明液体,易挥发,易水解。一中化学兴趣小组探究制备POCl3所需的装置如下图所示:

反应原理:PCl3+Cl2+H2O![]() POCl3+2HCl(PC13常温下为液态,易挥发)。
POCl3+2HCl(PC13常温下为液态,易挥发)。
(1)仪器3的名称是 _________,仪器2中装入的物质为______,仪器I的作用是_____.
(2)请选择上述必要装置并组装,用小写字母连接:________________________。
(3)开始通入氯气。同时慢慢滴加水,控制氯气和水的质量比在3.94左右,理由是:________________________.
(4)上述装置有一处不足,请指岀该不足:__________________________.
(5)上述反应剩余PCl3可以继续通入Cl2,再和P4O10反应,也可以产生的POC13 .。 写出该反应的化学方程式:__________________________________ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学实验中,通常利用如图所示的装置进行喷泉实验,来验证气体的“溶解性”,下列有关说法不正确的是

A.用滴管加入液体后,由于气体的“溶解”,使瓶内压强减小,导致瓶内压强小于外界压强,从而形成喷泉
B.选用合适的溶液,CO2也能做喷泉实验
C.HCl、NH3和SO2均能用该装置做喷泉实验
D.用NO2气体做喷泉实验,烧瓶中将充满稀硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com