
【题目】短周期元素X、Y、Z、W的原子序数依次增大。Z在短周期主族元素中原子半径最大;m、n、p、q为它们的单质;常温下,q为黄绿色气体,a为无色液体;各物质间转化关系如图所示。下列说法不正确的是

A. d中可能含有非极性共价键
B. Y、Z、W分别与X形成的化合物沸点:Z<Y<W
C. m在q中燃烧,产生大量白雾
D. 元素非金属性:Y>W>X
【答案】B
【解析】短周期元素X、Y、Z、W的原子序数依次增大。Z在短周期主族元素中原子半径最大,Z为Na元素;m、n、p、q为它们的单质;常温下,q为黄绿色气体,q为氯气;a为无色液体,a为水,则X为H元素、Y为O元素、W为Cl元素。根据流程图,m+n=水,m、n为氢气和氧气,q+m=c,则m为氢气,c为氯化氢,n为氧气,p为钠,因此b为氯化钠,d为氧化钠或过氧化钠。A.根据上述分析, d为氧化钠或过氧化钠,其中过氧化钠中含有非极性共价键,故A正确;B.水分子间能够形成氢键,水的沸点最高,故B错误;C. 氢气在氯气中燃烧,发出苍白色火焰,产生大量白雾,故C正确;D. 同主族从上到下,非金属性减弱;同周期从左向右,非金属性增强,另外,氧气与氯化氢能够反应生成氯气,因此元素的非金属性:O>Cl>H,故D正确;故选B。


 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源: 题型:
【题目】
汽车尾气中的氮氧化物气体是导致雾霾的要原因之一。请回答下列有关尾气治理的问题:
(1)用化学方程式解释汽车尾气中含有NO的原因_______________________________。
(2)汽车排气管内安装的催化转化器,可使汽车尾气中的主要污染物NO、CO转化为无毒的大气循环物质。
已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJmol-1
2C(s)+O2(g)=2CO(g) △H= -221.0kJmol-1
C(s)+O2(g)=CO2(g) △H= -393.5 kJmol-1
则分析反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的△H= ___________kJmol-1。
(3)将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中,在不同条件下反应过程中部分物质的浓度变化状况如图1所示。
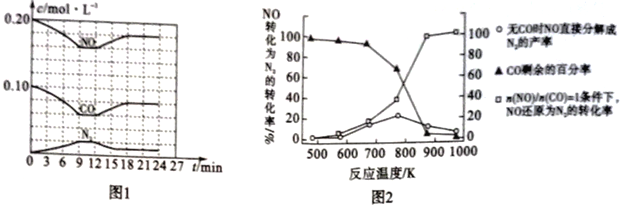
①计算反应在第9-12 min时的平衡常数K=____________。
②第12 min时改变的反应条件可能是_____________(任写一条)。
(4)某研究机构在实验室以Ag-ZSM-5为催化剂。测得单位时间内NO转化为N2的转化率随温度变化情况如图2所示。
①若不使用CO,发现当温度超过775 K时,NO的分解率降低,其可能的原因是________________。
②在n(NO)/n(CO) =1的条件下,为更好地除去NO,应控制的最佳温度应在____ K左右。
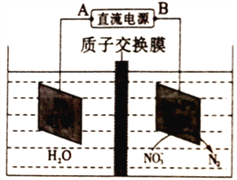
(5)氮氧化物进入水体可转化为NO3-,电化学降解法可用于治理水中NO3-的污染,原理如右图所示。则电源正极为______(选填“A”或“B”),阴极电极反应式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是
A. ClO2具有氧化性,可用于水的消毒杀菌
B. SO2具有还原性,可用于纸浆的漂白
C. MnO2具有氧化性,可用于H2O2制O2
D. SiO2能与强碱反应,可用于制光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取1.43 g Na2CO3·xH2O 溶于水配成10 mL 溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸 2.0 mL,并收集到112 mL CO2(标准状况)。
(1)Na2CO3·xH2O的摩尔质量为。
(2)稀盐酸物质的量浓度为。
(3)x值为 , 碳酸钠溶液的物质的量浓度为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将相同物质的量的甲烷和氯气混合后,在漫射光的照射下充分反应,生成物中物质的量最大的是( )
A.CH3Cl
B.CH2Cl2
C.CCl4
D.HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)CO(g)+H2(g)在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
A.增加C的量
B.将容器的体积缩小一半
C.保持容器体积不变,充入N2
D.保持容器体积不变,充入H2O(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油产品中除含有H2S外,还含有各种形态的有机硫,如COS、CH3SH等。
回答下列问题:
(1)CH3SH(甲硫醇)的电子式为__________。
(2)CO和H2S反应可产生羰基硫( COS)。在一恒容密闭容器中发生反应:CO(g)+H2S(g)![]() COS(g)+H2(g)并达到平衡,数据如下表所示:
COS(g)+H2(g)并达到平衡,数据如下表所示:
实验 | 温度/℃ | 起始时 | 平衡时 | |||
n(CO)/mol | n(H2S)/mol | n(COS)/mol | n(H2)/mol | n(CO)/mol | ||
1 | 150 | 10.0 | 10.0 | 0 | 0 | 7.0 |
2 | 150 | 7.0 | 8.0 | 2.0 | 4.5 | a |
3 | 400 | 20.0 | 20.0 | 0 | 0 | 16.0 |
①该反应是________反应(填“吸热”或“放热”)。
②实验1达平衡时,CO的转化率为_______。
③实验2达到平衡时,a_______7.0(填“大于”“小于”或“等于”)。
④实验3达平衡后,再充入1.0 molH2,平衡常数值____(填“增大”“减小”或“不变”)。
(3)COS是大气污染物。在酸性溶液中可用H2O2氧化COS生成一种强酸脱硫。该脱除反应的化学方程式为_______________。
(4)有一种脱硫工艺为:真空K2CO3一克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3 +H2S =KHS +KHCO3,该反应的平衡常数的对数值为lgK=_____(已知:H2CO3 lgK1=-6.4,lgK,2=- 10.3;H2S lgKl=-7.0,lgK2
②已知下列热化学方程式:
a. 2H2S(g)+3O2(g)=2SO2(g)+2H2O(1) △H1=-1172kJ/mol
b. 2H2S(g)+O2(g)=2S(s)+2H2O(1) △H2 = 632 kJ/mol
克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s),则该反应的热化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下在一容积恒定的密闭容器中,进行如下可逆反应:2A(g)+B(s) ![]() C(g)+D(g)。当下列物理量不再发生变化时,能表明该反应已达到平衡状态的是( )
C(g)+D(g)。当下列物理量不再发生变化时,能表明该反应已达到平衡状态的是( )
①容器内混合气体的密度②容器内混合气体的压强③容器内混合气体的总物质的量④容器内C物质的物质的量浓度
A.①④
B.②③
C.②③④
D.④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com