
【题目】用FeS2纳米材料制成的高容量锂电池,电极分别是二硫化亚铁和金属锂,电解液是含锂盐的有机溶剂。下列说法错误的是
A. 金属锂作电池的负极
B. 电池正极反应为FeS2+4Li++4e-==Fe+2Li2S
C. 放电时,Li+向负极迁移
D. 电池总反应为FeS2+4Li ==Fe+2Li2S
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列事故或药品的处理正确的是()
A. 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B. 眼睛里溅进了少量酸或碱溶液,要立即用大量水冲洗,边洗边眨眼睛
C. 不慎洒出的酒精在桌上燃烧起来,应立即用大量水扑灭
D. 将含硫酸的废液倒入水槽,用水冲入下水道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 聚氯乙烯塑料不可用来包装食品
B. 缺碘易患大脖子病
C. 由于淀粉在人体中会转化为氨基酸,因此每天都要摄入一定量的淀粉
D. 皮肤被烫伤或受浓硝酸腐蚀时,细胞结构将受到破坏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下图中的实验装置制取乙炔。

(1)制取乙炔的化学方程式是 .
(2)乙炔通入酸性KMnO4溶液中观察到的现象是 ,乙炔发生了 反应。
(3)乙炔通入溴的CCl4溶液中乙炔发生了 反应。
(4) 将21g CH4和C2H2的混合气体通入盛有足量溴水的容器中,溴水的质量增加了13g,则混合气体中CH4与C2H2的体积比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:苯和卤代烃在催化剂的作用下可以生成烷基苯和卤化氢,A是水果的催熟剂,C是生活中常见的有机物,乙苯能被酸性高锰酸钾溶液氧化为苯甲酸。几种物质之间的转化关系如图所示(生成物中所有无机物均已略去)。
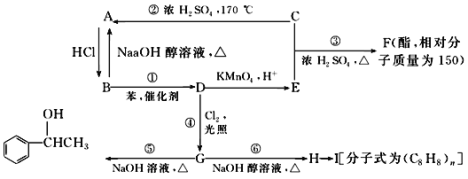
请回答下列问题:
(1)写出物质的结构简式:写出物质的结构简式:A____________,F_________,E__________。
(2)在①~⑥6个反应中,属于消去反应的是________(填编号)。
(3)写出下列反应的化学方程式:
①_____________________________;
②_____________________________;
⑥_____________________________。
H→I___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某学习小组通过实验研究Na2O2与水的反应。
操作 | 现象 |
向盛有4.0g Na2O2的烧杯中加入50mL蒸馏水 | 剧烈反应,产生能使带火星木条复燃的气体,得到的无色溶液a |
向溶液a中滴入两滴酚酞 | ⅰ.溶液变红 ⅱ.10分种后溶液颜色明显变浅,稍后,溶液变为无色 |
①Na2O2的电子式为 ,它与水反应的离子方程式是 。
②甲同学认为ⅱ中溶液褪色是溶液a中存在较多的H2O2,H2O2与酚酞发生了反应,并实验证实了H2O2的存在:取少量溶液a,加入试剂______ (填化学式),有气体产生。
(2)有一瓶澄清的溶液,可有含有大量的NO3-、Fe3+、NH4+、H+、K+、Mg2+、Al3+、SO42-、Ba2+、CO32-、Cl-、I-,现进行如下实验:
①测知溶液显酸性;
②取样加少量四氯化碳和数滴新制氯水,四氯化碳层溶液呈紫红色;
③另取样滴加稀NaOH溶液,使深液变为碱性,此过程中无沉淀生成;
④取少量上述碱性溶液,加Na2CO3溶液出现白色沉淀;
⑤将实验③中的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
由此可以推断:
溶液中肯定存在的离子有 。溶液中不能确定是否存在的离子有 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属镍在电池、合金、催化剂等方面应用广泛.
(1)下列关于金属及金属键的说法正确的是 .
a.金属键具有方向性与饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是 .
(3)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= .CO与N2结构相似,CO分子内σ键与π键个数之比为 .
(4)甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH).甲醇分子内C原子的杂化方式为 ,甲醇分子内的O﹣C﹣H键角 (填“大于”“等于”或“小于”)甲醛分子内的O﹣C﹣H键角.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com