
【题目】写出下列反应的化学方程式:(有机物必须写结构简式)
(1)工业生产TNT烈性炸药_______________________。
(2)2,3-二溴-2-甲基丁烷与NaOH醇溶液混合加热 。
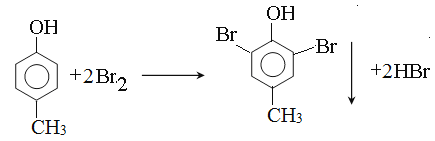
(3)对甲基苯酚与浓溴水反应 。
(4)葡萄糖与银氨溶液共热: 。
【答案】(1)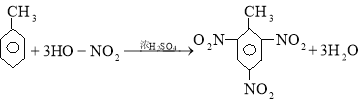
(2)CH3C(CH3)BrCHBrCH3+2NaOH![]() CH2=C(CH3)CH=CH2+2NaBr+2H2O
CH2=C(CH3)CH=CH2+2NaBr+2H2O
(3)
(4)HOCH2(CHOH)4CHO+2Ag(NH3)2OH![]() HOCH2(CHOH)4COONH4+2Ag↓+3NH3+H2O
HOCH2(CHOH)4COONH4+2Ag↓+3NH3+H2O
【解析】
试题分析:(1)工业利用甲苯和浓硝酸反应制备TNT烈性炸药,反应的方程式为
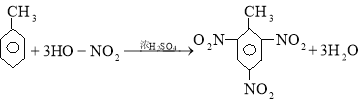 。
。
(2)2,3-二溴-2-甲基丁烷与NaOH醇溶液混合加热发生消去反应,方程式为CH3C(CH3)BrCHBrCH3+2NaOH![]() CH2=C(CH3)CH=CH2+2NaBr+2H2O。
CH2=C(CH3)CH=CH2+2NaBr+2H2O。
(3)对甲基苯酚与浓溴水发生取代反应的方程式为 。
。
(4)葡萄糖与银氨溶液共热的方程式为
HOCH2(CHOH)4CHO+2Ag(NH3)2OH![]() HOCH2(CHOH)4COONH4+2Ag↓+3NH3+H2O。
HOCH2(CHOH)4COONH4+2Ag↓+3NH3+H2O。


科目:高中化学 来源: 题型:
【题目】下列有关有机物的鉴别,不能实现的是( )
A. 用双缩脲试剂可区分蛋白质溶液和淀粉溶液
B. 用水可区分苯,甲苯和溴苯
C. 用高锰酸钾酸性溶液可区分乙烷和乙烯
D. 用溴水可鉴别苯酚溶液,2-己烯和甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式的划时代的意义。请回答下列问题:
(1)无机非金属材料
高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
![]()
①写出步骤Ⅰ的化学方程式:____________________________。
②步骤Ⅱ经过冷凝得到的SiHCl3(沸点为33.0 ℃)中含有少量的SiCl4(沸点为57.6 ℃)和HCl(沸点为-84.7 ℃),提纯SiHCl3的实验方法是____________________________。
(2)磁性材料
这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施对它的防护。最常见的铁制品腐蚀是电化学腐蚀,请写出最为普遍的电化学腐蚀的负极反应式:____________________________。
(3)激光材料
我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明:______________________________。
(4)高分子材料
它可以分成无机高分子材料和有机高分子材料。一种新型高效净水剂[AlFe(OH)nCl6-n]m就属于无机高分子材料,它广泛应用于生活用水和工业污水的处理,其中铁元素的化合价为__________;一种合成纤维腈纶,又称“人造羊毛”,以丙烯腈(CH2===CH—CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式:________________________。
(5)合金材料
14 g铜银合金与一定量某浓度的硝酸完全反应后,将放出的气体与1.12 L(标准状况下)O2混合通入水中,恰好全部被水吸收,则合金中铜的质量为________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.H2、SO2、CO2三种还原性气体都可用浓硫酸干燥
B.二氧化硫能使溴水褪色,说明二氧化硫具有漂白性
C.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+、无K+
D.向Na2O2与水完全反应后的溶液加入MnO2,产生氧气,是由于该溶液中含有H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去混在甲烷中的二氧化碳和水蒸气,可将混合气体先通过盛有__________(填物质名称,下同)的洗气瓶除去__________;再通过盛有__________的洗气瓶除去________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20 mL 0.2 mol /L H2A溶液中滴加0.2 mol /L NaOH溶液。有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示。根据图示判断,下列说法正确的是
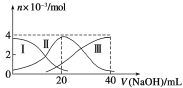
A.当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(A2-) >c(H+) >c(OH-)
B.等浓度的NaOH溶液与H2A溶液按2∶1混合后,其溶液中水的电离程度比纯水大
C.NaHA溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A)
D.向上述加入20 mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(己知硝酸只被还原为NO气体)。下列分析或结果错误的是
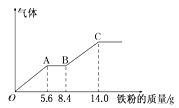
A. H2SO4浓度为2.5mol·L-1
B. OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C. 第二份溶液中最终溶质为FeSO4
D. 原混合酸中NO3-的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又属于吸热反应的是( )
A.铝片与稀盐酸反应
B.甲烷在氧气中燃烧
C.灼热的炭与二氧化碳反应
D.Ba(OH)28H2O与NH4Cl反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com