
 ����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã�
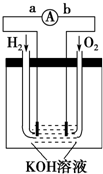
����ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�ã����� ��1��ԭ�����Ҫ�ǽ���ѧ��ת��Ϊ���ܣ�����ʧȥ���ӣ�Ϊ������������õ��ӣ�Ϊ�����������ɸ���ͨ����������������
��2������������ʧ���Ӻ����������ӷ�Ӧ����ˮ��
��3����Ӧ��Ӵ����Խ��Ӧ����Խ��
��4���ٸ��ݻ��ϼ۵ı仯�жϣ�
����LiH������ΪvL��������������ʵ������������������
�۸���ʵ�ʲμӷ�Ӧ�������Լ��缫��Ӧʽ���㣮
��� �⣺��1��ԭ�����Ҫ�ǽ���ѧ��ת��Ϊ���ܣ�ȼ�ϵ����ԭ��أ��ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�����ʧȥ���ӣ�Ϊ������������õ��ӣ�Ϊ�����������ɸ���ͨ��������������������a��b��
�ʴ�Ϊ����ѧ��ת��Ϊ���ܣ���a��b��
��2������������ʧ���Ӻ����������ӷ�Ӧ����ˮ���缫��ӦʽΪ2H2+4OH--4e-=4H2O����H2+2OH--2e-=2H2O����
�ʴ�Ϊ��2H2+4OH--4e-=4H2O����H2+2OH--2e-=2H2O����
��3����Ӧ��Ӵ����Խ��Ӧ����Խ�Ʋ�������缫��λ��������������������������ӿ�缫��Ӧ���ʣ�
�ʴ�Ϊ������缫��λ�������H2��O2���������ӿ�缫��Ӧ���ʣ�
��4����2Li+H2$\frac{\underline{\;\;��\;\;}}{\;}$2LiH���÷�Ӧ���ʧ���ӷ���������Ӧ��������ǻ�ԭ����LiH+H2O=LiOH+H2�����÷�Ӧ��H2O�õ�������������������ԭ��Ӧ������H2O����������
�ʴ�Ϊ��Li��H2O��
����LiH���ΪvL�����ʵ���Ϊn=$\frac{0.82��1000v}{8}$��mol�������ݷ�Ӧ����ʽ��2n��H2��=n��LiH������$\frac{0.82��1000v}{8}$��mol��=2��$\frac{224L}{22.4L/mol}$=20mol��v=$\frac{160}{820}$L��
�����յ�H2��������ɵ�LiH�����Ϊ224L��$\frac{160}{820}$L=1148��1��
�ʴ��ǣ�1148��1��
��20molLiH������20molH2��ʵ�ʲμӷ�Ӧ��H2Ϊ20mol��80%=16mol��1molH2ת����1molH2O��ת��2mol���ӣ�����16molH2��ת��32mol�ĵ��ӣ�
�ʴ�Ϊ��32��
���� ���⿼��ԭ���ԭ����Ϊ��Ƶ���㣬ԭ������ѵ��ǵ缫��Ӧʽ����д��Ҫ��ϵ������Һ�������д��ע�⣺��4����ת�Ƶ������ʵ���Ϊ������ȼ�ϵ��ʱת�Ƶ������ʵ�������������������ת�Ƶ������ʵ�����Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 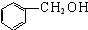 ����-OH ����-OH | B�� | 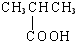 ����-CHO ����-CHO | ||
| C�� |  ȩ��-CHO ȩ��-CHO | D�� | CH3-O-CH3 ���� 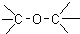 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
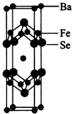 �������һ�ֳ����ĺϽ����£��ӹ����ܺã��������������й㷺��;��һ�ֲ���ֵ���Ҫ�ɷ���Fe��Ni��Cr��Si��P���ش��������⣺
�������һ�ֳ����ĺϽ����£��ӹ����ܺã��������������й㷺��;��һ�ֲ���ֵ���Ҫ�ɷ���Fe��Ni��Cr��Si��P���ش��������⣺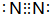 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
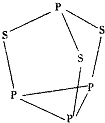 ��A��B��C��D��E����Ԫ�أ��������Ϣ���£�
��A��B��C��D��E����Ԫ�أ��������Ϣ���£�| Ԫ�� | �����Ϣ |
| A | AԪ�ص�һ��ԭ��û�����ӣ�ֻ��һ������ |
| B | B�ǵ縺������Ԫ�� |
| C | C�Ļ�̬ԭ��2p���������δ�ɶԵ��� |
| D | DΪ����Ԫ�أ�����Eͬ���ڣ�����������������˶�״̬��ͬ�ĵ��� |
| E | E���γ�ש��ɫ����ɫ����E2O��EO���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ�� | B�� | �ɼ�����ȡ�ȷ� | C�� | ����������ը | D�� | �ɼ�����ȡ̿�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢ݢߢ� | C�� | �٢ݢ� | D�� | �ݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH3�����к��зǼ��Լ� | B�� | CCl4�����к������Ӽ� | ||
| C�� | H2O������ֻ�м��Լ� | D�� | CO2������û�м��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
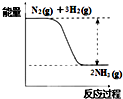 ���Ѿ����ֵ�һ�ٶ���Ԫ���У���ϡ�������⣬�ǽ���Ԫ��ֻ��ʮ���֣������������������е���ϵ��
���Ѿ����ֵ�һ�ٶ���Ԫ���У���ϡ�������⣬�ǽ���Ԫ��ֻ��ʮ���֣������������������е���ϵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com