
(9��)A��B��C��D��EΪԭ��������������Ķ�����Ԫ�ء���֪A��B��E��ԭ������㹲��11�����ӣ���������Ԫ�ص�����������Ӧ��ˮ����֮���������ܷ�Ӧ�����κ�ˮ��CԪ�ص������������ȴ�����������4��DԪ��ԭ�Ӵ�����������������������3����ش��������⣺
��1��д������Ԫ�ط��ţ�A________��C________��E________��
��2�� EԪ��+1�ۺ�����ĵ���ʽΪ��_________________��
��3��д��A��B��Ԫ������������Ӧ��ˮ�������Ӧ�����ӷ���ʽ______________��
��4���Ƚ�C��D����������Ӧˮ���������__________________��
��1��Na��Si��Cl ����1�֣��� ��3�� 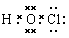 ��2�֣�
��2�֣�
��3��Al(OH)3��OH��=== AlO2����2H2O ��2�֣� ��4��H3PO4>H2SiO3 ��2�֣�
��������
������������������֪��A��Na��B��Al��C��Si��D��P��E��Cl����1��Ԫ�ط��ţ�A��Na��C��Al��E��Cl����2�� EԪ��+1�ۺ�����ĵ���ʽΪ��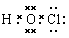 ����3�� A��B��Ԫ������������Ӧ��ˮ�������Ӧ�����ӷ���ʽ��Al(OH)3��OH��=== AlO2����2H2O������Ԫ�صķǽ�����P>Si��Ԫ�صķǽ�����Խǿ��������������Ӧ��ˮ��������Ծ�Խǿ����������H3PO4>H2SiO3��
����3�� A��B��Ԫ������������Ӧ��ˮ�������Ӧ�����ӷ���ʽ��Al(OH)3��OH��=== AlO2����2H2O������Ԫ�صķǽ�����P>Si��Ԫ�صķǽ�����Խǿ��������������Ӧ��ˮ��������Ծ�Խǿ����������H3PO4>H2SiO3��
���㣺����Ԫ�ص��ƶϡ�Ԫ�����ڱ���Ԫ�������ɵ�Ӧ�õ�֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�ϲ��и���8���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���������У��ȿ���Ũ�������ֿ��ù���NaOH�������
��Cl2����O2����H2����SO2����CO����NH3����CH4����NO2����CO2
A���ڢۢݢ� B���٢ۢߢ� C���ۢݢߢ� D���ڢۢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һ�ο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
ijͬѧʵ�鱨�������������ݣ��������ݲ���������
A����������ƽ��ȡ11.7 gʳ��
B������Ͳ��ȡ12.3 mL����
C���ù㷺pH��ֽ���ij��Һ��pHֵΪ3.6
D���ñ�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ��ȥ21.20 mL NaOH��Һ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ij��������һҺ�����ʱ��ƽ��ʱ����Ϊnml, ����ʱ����Ϊxml, ����ʱ����Ϊyml����y >n> x�������õ�����������
A������ƿ B����ʽ�ζ��� C����ʽ�ζ��� D����Ͳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ������ѧ�ڵ�һѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й��������������ȷ����
A. �ü��ȷֽ�ķ�������̼���ƺ�̼���������ֹ���
B������0.1000 mol��L-1����������Һʱ����Һ��ת�Ƶ�����ƿ�����ò���������
C. ����NH4+ʱ���������м���NaOH��Һ���ȣ���ʪ�����ɫʯ����ֽ�����ݳ�������
D����Һʱ����Һ©���Ķ���Ӧ��ʹ���ϰ��������С��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭����У������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ�ܱ������У���ӦaA(g) bB(g)��ƽ������¶Ȳ��䣬������������룬���ﵽ�µ�ƽ��ʱ��A��Ũ������Ϊԭ����1.8����������˵���������(����)
bB(g)��ƽ������¶Ȳ��䣬������������룬���ﵽ�µ�ƽ��ʱ��A��Ũ������Ϊԭ����1.8����������˵���������(����)
A��ƽ��������Ӧ�����ƶ���
B������A��ת����������
C�����º�ѹʱ�ٳ���A���ʣ��ﵽ�µ�ƽ��ʱA����������������
D��a��b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭����У������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ���������������
A����ʪ���pH��ֽ��ϡ��Һ��pH���ⶨֵƫС
B��������ƿ������Һ������ʱ���ӿ̶��ߣ�������ҺŨ��ƫС
C���ζ�ǰ�ζ����������ݣ��յ����ʱ�����ݣ��������ƫС
D���ⶨ�кͷ�Ӧ�ķ�Ӧ��ʱ��������������У������¶�ֵƫС
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����и���9��ѧ����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������Ԫ��X��Y��Z��W��Q��ԭ��������������X����̬�⻯�K������Y���⻯���У������£�Z�Ŀ�״����������W������������ˮ�����ϡ��Һ��ȴ��������Ũ��Һ������˵����ȷ����
A��Ԫ��Y����������ϼ�Ϊ+6
B�����Ӱ뾶�Ĵ�С˳��ΪW>Q>Z>X>Y
C����̬�⻯��ķе㣺Y>W
D��Ԫ��W������������Ӧ��ˮ�������Ա�Q��ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�콭��ʡ�����ظ߶���ѧ�����е��в��Ի�ѧ�Ծ��������棩 ���ͣ������
��18�֣���֪���淴ӦCO2(g) + H2(g) CO(g) + H2O(g)��
CO(g) + H2O(g)��
��д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��K= ��
��830Kʱ������ʼʱ��c (CO2)=2mol/L��c (H2)=3mol/L��ƽ��ʱCO2��ת����Ϊ60%��������ת����Ϊ ��KֵΪ ��
��830Kʱ����ֻ����ʼʱc (H2)��Ϊ6mol/L����������ת����Ϊ ��
����830Kʱ����ʼŨ��c (CO2) = a mol/L��c (H2) = b mol/L��H2O��ƽ��Ũ��Ϊc (H2O) = c mol/L����a��b��c֮��Ĺ�ϵʽ�� ���ڵ�a = bʱ��a = c��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com