
【题目】下列关于金属钠的叙述中,不正确的是
A.金属钠是银白色金属,硬度很大
B.在空气中加热时,金属钠剧烈燃烧,产生黄色火焰,生成过氧化钠
C.金属钠与水反应时,浮在水面,熔成小球,快速游动
D.由于金属钠易与空气中的成分发生化学反应,所以需要保存在煤油中
科目:高中化学 来源: 题型:
【题目】汉黄芩素(其结构如下图所示)是传统中草药黄芩的有效成分之一,对肿瘤细胞的杀伤有独特作用。下列有关汉黄芩素的叙述正确的是
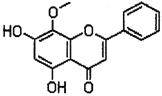
A. 汉黄芩素的分子式为C16H13O3
B. 汉黄芩素遇FeCl3溶液显色
C. lmol汉黄芩素与溴水反应,最多消耗2molBr2
D. 汉黄芩素与足量H2发生加成反应后,该分子中官能团的种类减少1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制硫酸的一步重要的反应是SO2在400-500℃下催化氧化反应: 2SO2+O2![]() 2SO3,该反应是个正反应放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中不正确的是
2SO3,该反应是个正反应放热的可逆反应。如果反应在密闭容器中进行,下列有关说法中不正确的是
A. 使用催化剂的目的是加快反应速率,提高生产效率
B. 在上述条件下,SO2不可能100%地转化为SO3
C. 增加O2的浓度,可以提高SO2的转化率
D. 当SO2和SO3的浓度相等时,反应一定达到平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一原电池的结构示意图,下列说法中,错误的是( ) 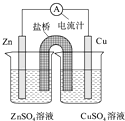
A.Cu电极为正电极
B.原电池工作时,电子从Zn电极流出
C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu
D.盐桥(琼脂﹣饱和KCl溶液)中的K+移向ZnSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年5月18日,中国国土资源部地质调查局宣布,我国在南海进行的可燃冰试采获得成功,成为全球第一个海域试采可燃冰成功的国家,可燃冰即天然气水合物,甲烷含量占80%至99.9%。化工生产中用甲烷和水蒸气反应得到以CO和H2为主的混合气体,这种混合气体可用于生产甲醇或合成氨,回答下列问题:
(1)对甲烷而言,有如下两个主要反应:
①CH4(g)+1/2O2(g)=CO(g)+2H2(g) △H1 =-36kJ·mol-1
②CH4(g)+H2O(g)=CO(g)+3H2(g) △H2 =+216kJ·mol-1
若不考虑热量耗散,物料转化率均为100%,最终炉中出来的气体只有CO、H2,为维持热平衡,每生产lmolCO,转移电子的数目为__________。
(2)甲醇是一种用途广泛的化工原料,工业上常用下列两种反应制备甲醇:
CO(g)+2H2(g)=CH3OH(g) △H1 =-90kJ·mol-1 K1
CO2(g)+3H2(g)= CH3OH(g)+H2O(l) △H2 K2
己知:CO(g)+H2O(g)= CO2(g)+H2(g) △H3 =-41.1kJ·mol-1 K3
H2O(l)=H2O(g) △H4 =+44.0kJ·mol-1 K4
则△H2=______ K2=_______ (用含K1、K3、K4的代数式表示)
(3)在一恒温恒容密闭容器中充入1molCO2和3molH2模拟工业合成甲醇的反应:CO2(g)十3H2(g) ![]() CH3OH(g)十H2O(g)
CH3OH(g)十H2O(g)
①下列能说明该反应已达到平衡状态的是______________________。
A.混合气体平均相对分子质量不变 B.混合气体密度不变
C.容器内压强恒定不变 D.反应速率满足以下关系:V正(CO2)=3V逆(H2)
E.CO2、H2、CH3OH、H2O物质的量浓度之比为1:3:1:1
F.单位时间内断裂3NAH-H键的同时形成2molH-O键
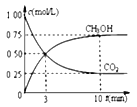
②模拟过程中测得CO2和CH3OH(g)浓度随时间变化如图所示,若此时容器内压强为P,则用平衡分压代替平衡浓度表示的化学平衡常数KP为_____________(用含P的代数式表示,数值保留两位小数),若此时再向容器内充入0.25molCO2和0.25molCH3OH的混合气体,则平衡______(填“正向“逆向“不”)移动。(已知:气体分压=气体总压×体积分数)
(4)甲醇可在电解银催化作用下制甲醛,从贵金属阳极泥中可提取“粗银”“粗银”(含Ag、Cu、Au)可用电解槽电解精炼,纯银作阴极,采用AgNO3和稀HNO3的混合液作电解液,阴极的主要电极反应式为_____。阴极还有少量副反应发生,产生的气体遇空气迅速变为红棕色,该副反应的电极反应式为_______。硝酸浓度不能过大,其原因是___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃按一定比例混合,在105℃时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L。下列各组混合烃中一定不符合此条件的是( )
A. CH4 C3H6 B. CH4 C2H4
C. C2H4 C3H4 D. C2H2 C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用海水可以提取溴和镁,提取过程如下:
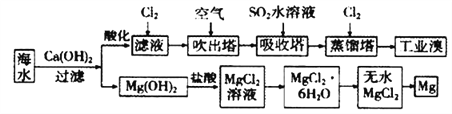
(1)提取溴的过程中,经过2次Br-→Br2转化的目的是________,吸收塔中发生反应的离子方程式是________________。
(2)据上述流程,将10m3海水中溴元素(海水中Br-离子含量为64mg/L)转化为工业溴,整个流程中至少需要标准状况下Cl2的体枳为______L(忽略Cl2溶解)。
(3)从理论上考虑,下列物质也能吸收Br2的是_____。
A.H2O B.FeCl2 C.Na2SO3
(4)由无水氯化镁得到镁的化学方程式是_______。
(5)有同学认为:可以加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,以简化实验步骤,体现实验的简约性原则,你是否同意该同学的观点,理由为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com