
【题目】利用海水可以提取溴和镁,提取过程如下:
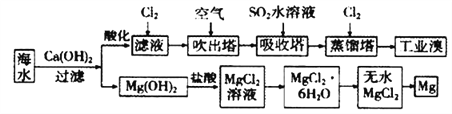
(1)提取溴的过程中,经过2次Br-→Br2转化的目的是________,吸收塔中发生反应的离子方程式是________________。
(2)据上述流程,将10m3海水中溴元素(海水中Br-离子含量为64mg/L)转化为工业溴,整个流程中至少需要标准状况下Cl2的体枳为______L(忽略Cl2溶解)。
(3)从理论上考虑,下列物质也能吸收Br2的是_____。
A.H2O B.FeCl2 C.Na2SO3
(4)由无水氯化镁得到镁的化学方程式是_______。
(5)有同学认为:可以加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,以简化实验步骤,体现实验的简约性原则,你是否同意该同学的观点,理由为_______________。
【答案】 对溴元素进行富集 ![]() 179.2 BC
179.2 BC ![]() 不同意,因为MgO熔点高,熔融时耗费大量的能量增加生产成本,所以观点不正确。
不同意,因为MgO熔点高,熔融时耗费大量的能量增加生产成本,所以观点不正确。
【解析】分析:海水中加入氢氧化钙沉淀镁离子后过滤,在滤液中通入氯气是将滤液中的Br-氧化为Br2,再利用热的空气将Br2吹出,进入吸收塔与SO2反应生成溴离子;再通入氯气将Br-氧化为Br2,两次转化的目的是对溴元素进行富集;氢氧化镁加入盐酸溶解得到氯化镁溶液,氯化镁溶液中得到氯化镁晶体的操作是加热蒸发冷却结晶得到无水氯化镁,电解熔融氯化镁得到金属,据此解答。
详解:(1)根据以上分析可知经过2次Br-→Br2转化的目的是得到更多的溴单质,提取过程对溴元素进行富集;吸收塔内通入的是二氧化硫气体是和溴单质反应生成溴离子,因此吸收塔中反应的离子方程式为;SO2+Br2+2H2O=4H++2Br-+SO42-;
(2)若将10m3海水中的溴元素转化为工业溴,依据溴元素含量为64mg/L可计算10m3海水中含溴元素的质量是10000L×64g/L×10-3=640g;物质的量=640÷80g/mol=8mol,依据反应计算得到:2Br-+Cl2=Br2+2Cl-,消耗氯气物质的量为:4mol;提取过程中需要两次通入氯气实现溴离子被氧化,所以至少需要标准状况下Cl2的物质的量为8 mol,在标准状况下体积为8mol×22.4L/mol=179.2L;
(3)A.单质溴H2O中的溶解度很小,A错误;B.FeCl2具有还原性,能被溴氧化,因此可以吸收溴,B正确;C.Na2SO3具有还原性,能被溴氧化,因此可以吸收溴,C正确。答案选BC;
(4)镁是活泼的金属,电解熔融氯化镁得到金属镁和氯气,因此由无水氯化镁得到镁的化学方程式是MgCl2(熔融)![]() Mg+Cl2↑。
Mg+Cl2↑。
(5)由于MgO熔点高,熔融时耗费大量的能量增加生产成本,所以观点不正确。


科目:高中化学 来源: 题型:
【题目】下列关于金属钠的叙述中,不正确的是
A.金属钠是银白色金属,硬度很大
B.在空气中加热时,金属钠剧烈燃烧,产生黄色火焰,生成过氧化钠
C.金属钠与水反应时,浮在水面,熔成小球,快速游动
D.由于金属钠易与空气中的成分发生化学反应,所以需要保存在煤油中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一铁、铜混合物粉末平均分成三等份,分别加入到同浓度、不同体积的稀硝酸中,充分反应后,收集到NO气体的体积及剩余固体的质量如表 (设反应前后溶液的体积不变,气体体积已换算为标准状况时的体积):
实验序号号 | 稀硝酸的体积/mL | 剩余固体的质量/g | NO的体积/L |
① | 100 | 17.2 | 2.24 |
② | 200 | 8.00 | 4.48 |
③ | 400 | 0 | V |
下列说法正确的是( )
A.表中 V=7.84 L
B.原混合物粉末的质量为25.6 g
C.原混合物粉未中铁和铜的物质的量之比为2:3
D.实验3所得溶液中硝酸的物质的量浓度为0.875 molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏伽德罗常数为NA . 下列说法正确的是( )
A.0.1 mol C2H6O分子中含有C﹣H键数为0.5NA
B.标准状况下,11.2 L CH3CH2OH中含有的分子数目为0.5NA
C.3.0 g甲醛(HCHO)和乙酸的混合物中含有的原子总数为0.4NA
D.常温常压下,12 g冰醋酸溶解于水,其电离出的氢离子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.糖类、油脂、蛋白质都能发生水解反应
B.糖类、油脂、蛋白质都是由C,H,O三种元素组成的
C.糖类、油脂、蛋白质都是高分子化合物
D.油脂有油和脂肪之分,但都属于酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上用废镍催化剂(成分主要为Ni ,含有一定量的Al2O3、Fe、SiO2、CaO等)制备草酸镍晶体的流程如图所示:
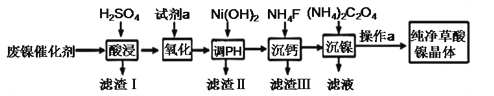
已知:①相关金属离子生成氢氧化物沉淀的pH见表中数据:
金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
②Ksp(NiC2O4)= 4.05×1010
(1)“酸浸”前将废镍催化剂粉碎的目的是:____。“滤渣Ⅰ”的主要成分为:____。
(2)若试剂a为H2O2 ,写出氧化时反应的离子方程式:____。
(3)调节pH的范围为:____。
(4)写出“沉钙”操作中加入NH4F时发生反应的离子方程式:____,NH4F的电子式为:____。
(5)如果“沉镍”操作后测得滤液中C2O42 的浓度为0.18 mol·L1,则溶液中c(Ni2+)= ____ mol·L1。
(6)将得到的草酸镍晶体在真空中加热至320℃分解,可重新制得单质镍催化剂。该制备过程的化学方程式为:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物在氧气中充分燃烧,生成CO2和H2O的物质的量之比为1:2,则该有机物
A.一定含有C、H、O三种元素B.分子中C、H原子个数之比为1:4
C.只含有C、H两种元素D.最简式为CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列广告用语在科学性上错误的是( )
A.没有水就没有生命
B.这种蒸馏水绝对纯净,其中不含任何离子
C.这种口服液含丰富的氮、磷、锌等微量元素
D.这种饮料不含任何化学物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO+H2的混合气体又称“合成气”,在合成有机物中应用广泛。工业上常采用天然气与水蒸气或二氧化碳反应等方法来制取合成气。请回答下列问题:
(1)已知在一定条件下,0.25molCH4 与水蒸气完全反应制备“合成气”时吸收51.5kJ 的热量,请写出该反应的热化学方程式__________________________________________________。
(2)天然气与CO2反应也可制备合成气,在10L 密闭容器中通入lmolCH4 与1molCO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示。
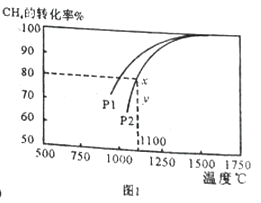
①1100℃、P2时气体混合后反应经过10min 至x 点的平衡,用CO 的变化量表示反应速率v(CO)=_____________;
②下列选项中能表示该反应已达到平衡状态的是____________;
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.c(CH4)=c(CO)
③由图1可知,压强P1_______P2 (填“大于”或“小于”);压强为P2时,在y点: v(正)____ v(逆) (填“大于”“小于”或“等于”)。求y点对应温度下的该反应的平衡常数K= __________。
(3)天然气中的H2S 杂质常用氨水吸收,产物为NH4HS。
已知: 25℃时,NH3·H2O 的电离常数K=1.8×10-5,H2S 的两步电离常数分别为Ka1=1.3×10-7,Ka2=7.1×10-15。求NH4HS溶液中离子浓度大小关系_____________________(由大到小)。
(4)合成气制甲醚的反应方程式为2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
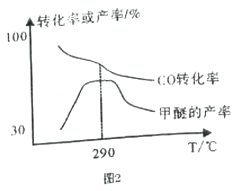
①290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是___________________________;
②b______0 (填“ >”或“<”或“=”) ,理由是___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com