
| ʱ��/���ʵ��� | n��A����mol�� | n��B����mol�� | n��C����mol�� | n��D����mol�� |
| ��ʼ | 0.9 | 1.4 | 0 | 0.2 |
| ��1min | 0.6 | 1.1 | 0.15 | |
| ��2min | 0.4 | 0.9 | 0.25 | |
| ��3min | 0.3 | 0.8 | 0.8 | |
| ��4min | 0.3 | 0.8 | 0.3 | 0.8 |
| ��5min | 0.35 | 0.85 | 0.275 | 0.75 |
| ��c |
| ��t |
| 1.4mol-0.9mol |
| 1L |
| 0.5mol/L |
| 2min |
| 0.6mol |
| 0.9mol |
| m |
| V |


 �����ҵ���������ϵ�д�
�����ҵ���������ϵ�д� �����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д�
�����̸�Ӯ����ٸ�Ч�����ܸ�ϰ���ϿƼ�������ϵ�д� �����ҵ�����������ѧ���ӳ�����ϵ�д�
�����ҵ�����������ѧ���ӳ�����ϵ�д� ����ѧ��Ӯ�����ϵ�д�
����ѧ��Ӯ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
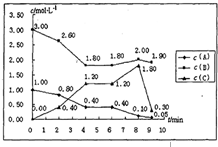 ��һ���ݻ��̶�Ϊ1L���ܱ������У�������ӦmA��g��+nB��g���TpC��g����H=������Ӧ�������ͼ��ʾ��
��һ���ݻ��̶�Ϊ1L���ܱ������У�������ӦmA��g��+nB��g���TpC��g����H=������Ӧ�������ͼ��ʾ��| 10 |
| 9 |
| 10 |
| 9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�����ʡƽ��ɽ�и߶���ѧ����ĩ���������ۺϻ�ѧ�Ծ����������� ���ͣ������
(13��)һ�������·�����Ӧ��CO2(g)+3H2(g) CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й����е������仯��
CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й����е������仯��
��1��ͼ������ (�a����b��)��ʾʹ�ô���ʱ�ķ�Ӧ���̡�ʹ�ô����Ը÷�Ӧ��Ӱ����______(��ѡ����ĸ)��
| A����߷�Ӧ���� | B�����CO2��ת���� |
| C�����ͷ�Ӧ��� | D���ı䷴Ӧ�Ħ�H |
 CH3OH(g)+H2O(g)�Ļ�ѧƽ�ⳣ���ı���ʽK=_________�������¶ȣ�Kֵ��_______(���������С�����䡱)��
CH3OH(g)+H2O(g)�Ļ�ѧƽ�ⳣ���ı���ʽK=_________�������¶ȣ�Kֵ��_______(���������С�����䡱)�� CH3OH(g)+H2O(g)�Ħ�H="_____" kJ��mol��1
CH3OH(g)+H2O(g)�Ħ�H="_____" kJ��mol��1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и߶���ѧ��ĩ���Ի�ѧ�Ծ��������棩 ���ͣ������
�ڳ��¡���ѹ�����������£�N2�ڴ���������ˮ�������з�Ӧ��
2N2 (g)+6H2O (l)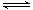 4NH3 (g)+3O2 (g)
��H�� a kJ��mol��1
4NH3 (g)+3O2 (g)
��H�� a kJ��mol��1
������ӦNH3���������¶ȵĹ�ϵ����ѹ�´ﵽƽ��ʱ��ò���ʵ���������±���
|
�¶� T/K |
303 |
313 |
323 |
|
NH3������/(10��6 mol) |
4.8 |
5.9 |
6.0 |
��1���˺ϳɷ�Ӧ��a 0 (�����������������)��
��2����ˮϡ��0.1 mol��L��1��ˮ����ϡ��ʱ��Һ�¶Ȳ��䣩������Һ������ˮ�������Ӷ���С�������е� ������ţ���
A��c(NH3��H2O)
B��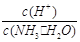 C��c(H+)��c(OH��)
D��
C��c(H+)��c(OH��)
D��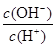
��3����ҵ�ð���ȡ�����������ӦΪ��4NH3(g)+5O2(g)
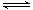 4NO(g)+6H2O(g)
��H��0������ʼ�����ʵ�����ͬ�������й�ϵͼ��ȷ����________(�����)��
4NO(g)+6H2O(g)
��H��0������ʼ�����ʵ�����ͬ�������й�ϵͼ��ȷ����________(�����)��
A B C D
��4����1L�ݻ��̶����ܱ������з���������Ӧ���������ʵ����ʵ���Ũ�����±���
|
ʱ��/Ũ�� |
c(NH3) (mol/L) |
c(O2 ) (mol/L) |
c(NO) (mol/L) |
|
��ʼ |
0.8000 |
1.600 |
0.000 |
|
��4 min |
0.3000 |
0.9750 |
0.5000 |
|
��6 min |
0.3000 |
0.9750 |
0.5000 |
|
��8 min |
0.7000 |
1.475 |
0.1000 |
��Ӧ�ڵ�6 min��8minʱ�ı����������ı������������___________________���ڸ������£�ƽ����_______�ƶ�(����ҡ�)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�����ʡƽ��ɽ�и߶���ѧ����ĩ���������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
(13��)һ�������·�����Ӧ��CO2(g)+3H2(g) CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й����е������仯��
CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й����е������仯��
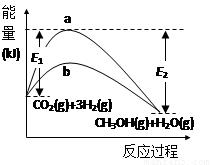
��1��ͼ������ (�a����b��)��ʾʹ�ô���ʱ�ķ�Ӧ���̡�ʹ�ô����Ը÷�Ӧ��Ӱ����______(��ѡ����ĸ)��
A����߷�Ӧ���� B�����CO2��ת����
C�����ͷ�Ӧ��� D���ı䷴Ӧ�Ħ�H
��2��CO2(g)+3H2(g) CH3OH(g)+H2O(g)�Ļ�ѧƽ�ⳣ���ı���ʽK=_________�������¶ȣ�Kֵ��_______(���������С�����䡱)��
CH3OH(g)+H2O(g)�Ļ�ѧƽ�ⳣ���ı���ʽK=_________�������¶ȣ�Kֵ��_______(���������С�����䡱)��
��3���ú�E1��E2�ı���ʽ��ʾCO2(g)+3H2(g) CH3OH(g)+H2O(g)�Ħ�H=_____ kJ��mol��1
CH3OH(g)+H2O(g)�Ħ�H=_____ kJ��mol��1
��4��һ���¶��£������Ϊ2L���ݻ��̶����ܱ������У�����2molCO2��6molH2����10min��Ӧ�ﵽƽ��״̬W������1molCH3OH��CO2��ת����Ϊ________���ӷ�Ӧ��ʼ��ƽ�⣬��H2��Ũ�ȱ仯��ʾ��ƽ����Ӧ����v(H2)=____________�����¶��£������Ϊ1L���ݻ��̶����ܱ������У����淴Ӧ��ʼ������ѧƽ�⣬�Ҹ���ֵ�ƽ��Ũ����ƽ��״̬W��ȫ��ͬ������ʼʱ����������n(CH3OH)=________��n(H2O)=________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com