
【题目】pC类似pH,是指稀溶液中溶质物质的量浓度的负对数。如某溶液溶质的浓度为1×10-3mol/L,则该溶液中溶质的pC=3。下列叙述正确的是
A.某温度下,任何电解质的稀溶液中,pC(H+)![]() pC(OH-)
pC(OH-)![]()
B.0.01mol/L的CaCl2溶液中逐滴加入纯碱溶液,滴加过程中pC(Ca2+)逐渐增大
C.0.01mol/L的BaCl2溶液中,pC(Cl-)![]() 2pC(Ba2+)
2pC(Ba2+)
D.用0.01mol/L的盐酸滴定某浓度的NaOH溶液,NaOH溶液的pC(OH-)逐渐减小
【答案】B
【解析】
根据题意,pC类似pH,不同温度下水的电解程度不同,对应的离子的物质的量浓度不同;氯化钙与碳酸钠反应产生碳酸钙沉淀和氯化钠,钙离子浓度逐步降低;氯化钡是强电解质,能完全电离;盐酸滴定氢氧化钠,发生中和反应,氢氧根浓度降低。
A、常温下电解质的稀溶液中,pC(H+) +pC(OH-)=14,不是任何温度,A错误;
B、0.01mol/L的氯化钙溶液中,加入碳酸钠溶液,则碳酸根离子与钙离子结合为碳酸钙沉淀,钙离子的物质的量浓度逐渐减小,则其负对数逐渐增大,B正确;
C、0.01mol/L的氯化钡溶液中,氯离子物质的量浓度是钡离子物质的量浓度的2倍,则pC(Cl-)=-lg[2C(Ba2+)],C错误;
D、用0.01mol/L的盐酸滴定某浓度的NaOH溶液,氢氧根离子的物质的量浓度逐渐减少,则氢氧根离子的pC值逐渐增大,D错误。
答案为B。


科目:高中化学 来源: 题型:
【题目】在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得出相应结论的是( )
选项 | 方法 | 现象 | 结论 |
A | 观察氯水颜色 | 氯水呈黄绿色 | 氯水中含Cl2 |
B | 向饱和NaHCO3溶液中加入足量氯水 | 有无色气体产生 | 氯水中含HClO |
C | 向红色纸条上滴加氯水 | 红色纸条褪色 | 氯水具有漂白性 |
D | 向FeCl2溶液中滴加氯水 | 溶液变成棕黄色 | 氯水具有氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产、环境等密切相关。下列说法错误的是
A.煤的液化、石油的裂化和油脂的皂化都属于化学变化
B.棉、丝、毛、油脂都是天然有机高分子化合物
C.乙烯与氧气在银催化作用下生成环氧乙烷原子利用率为100%
D.海水淡化的方法有蒸馏法、电渗析法等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.燃烧热和中和热的数值都会随反应物的用量不同而改变,故1molS(s)和2molS(s)的燃烧热不相等
B.已知:2C(s)+2O2(g)=2CO2(g) ΔH=akJ/mol,2C(s)+O2(g)=2CO(g)ΔH=bkJ/mol,则a>b
C.H2(g)的燃烧热为285.8kJ/mol,则表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l)ΔH=-571.6kJ/mol
D.反应NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57kJ/mol,在低温条件下不能自发进行,但在高温条件下能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫能起漂白、保鲜作用,使物品颜色显的白亮、鲜艳。如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。下列有关说法正确的是
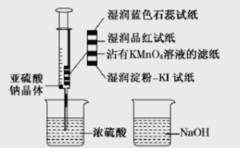
A.蓝色石蕊试纸变红后褪色
B.NaOH溶液可用于除去实验中多余的SO2
C.湿润淀粉-KI试纸未变蓝,说明SO2有还原性
D.品红试纸、沾有KMnO4溶液滤纸均褪色,证明了SO2的漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,回答下列问题:

(1)在这些元素中,_____(用元素符号填写,下同)是最活泼的金属元素;_____是最活泼的非金属元素,它们组成的化合物含有的化学键类型为_____。
(2)这些元素的最高价氧化物的对应水化物中_____酸性最强;_____碱性最强;能形成两性氢氧化物的元素是_____。
(3)写出①的最高价氧化物的化学式_____,电子式_____。
(4)③和氢元素组成的化合物中,既含有极性共价键又含有非极性共价键的化合物是_____。
(5)比较⑤与⑥的化学性质,_____更活泼,试用实验证明此现象_____(简述操作、现象和结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中氧原子数目与6.8gH2O2中氧原子数目一定相等的是( )
A.6.72 L COB.6.6 g CO2C.8 g SO3D.9.8 g H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种肼燃料电池的结构如图所示,下列说法正确的是( )
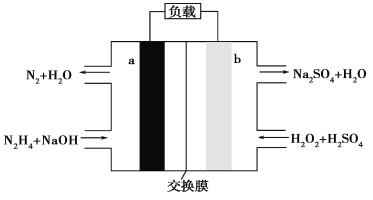
A. a极是正极,电极反应式为N2H4-4e-+4OH-=N2↑+4H2O
B. 电路中每转移NA个电子,就有1mol Na+穿过膜向正极移动
C. b极的电极反应式为H2O2+2e-=2OH-
D. 用该电池作电源电解饱和食盐水,当得到0.1mol Cl2时,至少要消耗0.1mol N2H4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法不正确的是![]()
A.“酸雨”、“臭氧层受损”、“光化学烟雾”都与氮氧化物有关
B.PM2.5作为空气质量预报的一项重要指标,它是指空气中直径小于或等于2.5m的颗粒物,该值越高,代表空气污染程度越严重
C.静电除尘治理悬浮颗粒污染,其依据是胶体的电泳原理
D.为消除碘缺乏症,卫生部规定食盐中必须加含碘物质,食盐中所加含碘物质是KI
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com