
【题目】某100mL溶液可能含有Na+、NH4+、Fe3+、CO32﹣、SO42﹣、Cl﹣中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出) 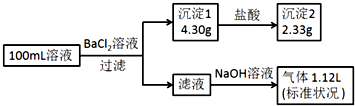
下列说法正确的是( )
A.原溶液中c(Cl﹣)≥0.1molL﹣1
B.取滤液,加硝酸银溶液,若产生白色沉淀,证明原溶液中存在Cl﹣
C.原溶液一定存在CO32﹣和SO42﹣ , 一定不存在Na+
D.原溶液可能存在Cl﹣ , 不存在Fe3+
【答案】A
【解析】解:加入氯化钡溶液,生成沉淀,一定含有碳酸根或是硫酸根中的至少一种,则该沉淀为BaSO4、BaCO3中的至少一种,沉淀部分溶解于盐酸,所以一定是BaSO4、BaCO3的混合物,一定存在CO32﹣、SO42﹣ , 硫酸钡沉淀是2.33g,物质的量是 ![]() =0.01mol,碳酸根离子的物质的量是
=0.01mol,碳酸根离子的物质的量是 ![]() mol=0.01mol,碳酸根和铁离子不共存,一定不存在Fe3+ , 所得到的滤液中加入氢氧化钠,出现气体,为氨气,一定含有铵根离子,根据元素守恒,铵根离子的物质的量是
mol=0.01mol,碳酸根和铁离子不共存,一定不存在Fe3+ , 所得到的滤液中加入氢氧化钠,出现气体,为氨气,一定含有铵根离子,根据元素守恒,铵根离子的物质的量是 ![]() =0.05mol,A.阳离子所带正电荷的物质的量之和:0.05mol,阴离子所带负电荷的物质的量之和=0.01×2+0.01×2=0.04mol,所以一定存在氯离子,如不含钠离子,则n(Cl﹣)=0.01mol,所以c(Cl﹣)=0.1molL﹣1 . 如含有钠离子,则n(Cl﹣)>0.01mol,所以c(Cl﹣)>0.1molL﹣1 . 故A正确;
=0.05mol,A.阳离子所带正电荷的物质的量之和:0.05mol,阴离子所带负电荷的物质的量之和=0.01×2+0.01×2=0.04mol,所以一定存在氯离子,如不含钠离子,则n(Cl﹣)=0.01mol,所以c(Cl﹣)=0.1molL﹣1 . 如含有钠离子,则n(Cl﹣)>0.01mol,所以c(Cl﹣)>0.1molL﹣1 . 故A正确;
B.由于加入氯化钡,引入氯离子,则不能证明原溶液是否含有氯离子,故B错误;
C.不能确定是否含有钠离子,故C错误;
D.由以上分析可知一定含有氯离子,故D错误.
故选A.


科目:高中化学 来源: 题型:
【题目】下列叙述中,正确的是( )
A.氯气不溶于水,因此可用排水法收集氯气
B.新制氯水可以使干燥的有色布条退色
C.因为氯气具有刺激性气味,所以可以杀死细菌和病毒
D.氢气在氯气中燃烧产生淡蓝色火焰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是( )
A.在离子化合物中也可能存在共价键
B.非金属的原子之间形成的化学键一定是共价键
C.含共价键的化合物不一定是共价化合物
D.含离子键的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于阿伏伽德罗常数的说法正确的是( )
A.阿伏伽德罗常数是12g14C中所含的碳原子数
B.阿伏伽德罗常数是0.012kg12C中所含的质子数
C.阿伏伽德罗常数是6.02×1023mol﹣1
D.阿伏伽德罗常数的符号为NA , 近似值为6.02×1023mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年10月,屠哟哟获得诺贝尔生理学或医学奖,理由是她发现了青蒿素,这种药品可以有效降低疟疾患者的死亡率.她成为首获科学类诺贝尔奖的中国人.青蒿素两步可合成得到治疗疟疾的药物青蒿琥酯.下列有关说法正确的是( )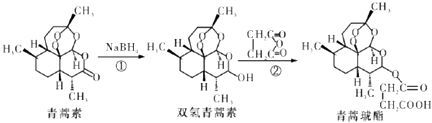
A.青蒿素分子式为C15H24O5
B.反应②原子利用率为100%
C.该过程中青蒿素生成双氢青蒿素属于氧化反应
D.1 mol青蒿琥酯与氢氧化钠溶液反应,最多消耗1 mol氢氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取100mL等物质的量浓度的硝酸和硫酸混合溶液,当加入200mL 1.5molL﹣1的Ba(OH)2溶液时,溶液显中性.请计算:
(1)原混合液中H+的物质的量浓度为molL﹣1 .
(2)当原混合液中加入0.5molCu,最终剩余铜的质量为g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿酸是合成青蒿素的原料,其结构如图所示.下列有关青蒿酸的说法正确的是( )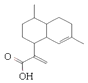
A.青蒿素分子式为:C15H20O2
B.1 mol青蒿酸可与3 mol H2发生加成反应
C.在一定条件,可与乙醇发生酯化反应
D.能使溴水褪色,不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组用打磨过的铝片进行如下实验,下列分析不合理的是

A. ①中铝片发生了钝化
B. ②中产生的气泡可能是氮氧化合物
C. ③中沉淀溶解的离子方程式是Al(OH)3+ OH-=AlO2- + 2H2O
D. ②中加水稀释过程中,仅发生了氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com