
����Ŀ�����ݻ��̶����ܱ������д��ڷ�Ӧ��A(g)+3B(g)![]() 2C(g) ��H<0ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬������ʵ�������������й�ϵͼ��
2C(g) ��H<0ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬������ʵ�������������й�ϵͼ��

�����ж���ȷ����
A. ͼI�о����Dz�ͬ�����Է�Ӧ��Ӱ�죬����ʹ�õĴ���Ч�ʽϸ�
B. ͼ���о������¶ȶԷ�Ӧ��Ӱ�죬�Ҽ��¶Ƚϸ�
C. ͼ���о�����ѹǿ�Է�Ӧ��Ӱ�죬�Ҽ�ѹǿ�ϴ�
D. ͼ���о����Dz�ͬ�����Է�Ӧ��Ӱ�죬�Ҽ�ʹ�õĴ���Ч�ʽϵ�
���𰸡�B
��������
�÷�Ӧ��һ�����������С�ķ��ȷ�Ӧ��ʹ�ô��������Ч�ʽϸߡ������¶ȡ�����ѹǿ����Ӧ���ʿ죬�ȴﵽƽ�⣬���������ƽ�ⲻ�����ƶ��������¶ȣ�ƽ�����淴Ӧ�����ƶ�������ѹǿ��ƽ��������Ӧ�����ƶ���
A��ҵ���ƽ��ʱ��̣�������ʹ�õĴ���Ч�ʽϸߣ����������ƽ�ⲻ�����ƶ����ﵽƽ��ʱC��Ũ��Ӧ��ȣ���A����
B�����ƽ��ʱ��̣����Լ��¶Ƚϸߣ�����Ӧ���ȣ������¶ȣ�ƽ�����淴Ӧ�����ƶ�������B��ת���ʼ�С����B��ȷ��
C�����ƽ��ʱ��̣����Լ�ѹǿ�ϸߣ�����ѹǿƽ��������Ӧ�����ƶ���ƽ��ʱ����B��ת����Ӧ�����ң���C����
D����������ƽ�ⲻ�����ƶ�������ƽ��ʱ��̣����Լ�ʹ�õĴ���Ч�ʽϸߣ���D����
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ʳͭ��Ǧ���ж���Ӧ��ȡ�ļ��ȴ�ʩ�ǣ� ��
A.���ô�����������ˮB.���ô�����ţ��
C.���ô�����ʳ��ˮD.�÷�������ʳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС����Ʋ�ͬʵ�鷽���Ƚ�Cu2+��Ag+ �������ԡ�
�������ϣ�Ag+ + I- = AgI�� K1 =1.2��1016��2Ag+ + 2I- = 2Ag��+ I2 K2 = 8.7��108
��1������1��ͨ���û���Ӧ�Ƚ�
���ữ��AgNO3��Һ����ͭ˿��������ɫ���壬��Һ������˵��������Ag+��Cu2+����Ӧ�����ӷ���ʽ��___________________________________________________��
��2������2��ͨ��Cu2+��Ag+ �ֱ���ͬһ���ʷ�Ӧ���бȽ�
ʵ�� | �� �� | ��ż����� | |
�� �� | �� �� | ||
| 1.0 mol/L KI��Һ | 1.0 mol/L AgNO3��Һ | ������ɫ��������Һ��ɫ |
1.0 mol/L CuSO4��Һ | ������ɫ����A����Һ��� | ||
�پ����飬������Һ����I2����ɫ������________��
�ھ����飬������Һ��I2���Ʋ�Cu2+������������ɫ����A��CuI��ȷ��A��ʵ�����£�
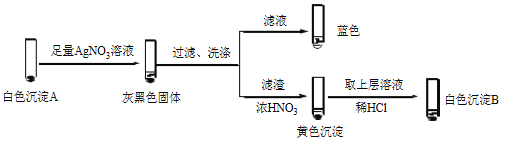
a��������Һ��I2����Һ����ɫ˵����Һ����________�������ӷ��ţ���
b����ɫ����B��________��
c����ɫ����A��AgNO3��Һ��Ӧ�����ӷ���ʽ��___________��˵��������Ag+��Cu2+��
��3����������2��Ag+ δ������I- ����Cu2+������I-��ԭ�����ʵ�����£�
��� | ʵ��1 | ʵ��2 | ʵ��3 |
ʵ�� |
KI��Һ |
KI��Һ AgNO3��Һ a b |
KI��Һ CuSO4��Һ c d |
���� | �����Ա仯 | a����Һ�Ͽ���ػ�ɫ,b�е缫����������������ָ��ƫת | c����Һ������dz��ɫ�� ������ָ��ƫת |
���缫��Ϊʯī����ҺŨ�Ⱦ�Ϊ 1 mol/L��b��d����ҺpH��4��
��a����Һ���ػ�ɫ��ԭ����___________________________���õ缫��Ӧʽ��ʾ����
�ڡ�ʵ��3������˵��Cu2+������I-�������ǿ����е�����Ҳ���������ã����ʵ��֤ʵ�˸����ݣ�ʵ�鷽����������_____________________________��
�۷���2�У�Cu2+������I-,��Ag+δ������I-����ԭ��һ�Ǵ�Kֵ______�����Ǵ�Cu2+�ķ�Ӧ�ص�______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪԪ�����ڱ��ж����ڵ�һ���֣�����Ԫ�ؾ�Ϊ��ϡ������Ԫ�ء����й���������Ԫ�ؼ��仯�����˵������ȷ����

A. ԭ�Ӱ뾶��W>Z>Y>X
B. ��̬�⻯����ȶ��ԣ�W<Z<X<Y
C. Z������������ˮ�������Ϊǿ��
D. W����������ϼ��븺���ϼ۵ľ���ֵ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ͬ�ļס������������У��ֱ����2 mol SO2��1mol O2������ͬ���¶��·�����Ӧ2SO2��O2![]() 2SO3�����ﵽƽ�⣬�ڸù����У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp��������������SO2��ת����Ϊ
2SO3�����ﵽƽ�⣬�ڸù����У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp��������������SO2��ת����Ϊ
A. ����p��B. ����p��C. С��p��D. ���ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԪ�ص�һ��ͬλ��Xԭ�ӵ�������ΪA������2Hԭ�����2HmX���ӣ��˷��Ӻ�N�����ӣ���a g 2HmX���������ӵ����ʵ�����
A. ![]() (A��N��m) molB.
(A��N��m) molB. ![]() (A��N) mol
(A��N) mol
C. ![]() (A��N��m) molD.
(A��N��m) molD. ![]() (A��N+2m) mol
(A��N+2m) mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�ɢϵ�ܲ��������ЧӦ����
A. ϡ���� B. ������Һ C. ������������ D. ����ͭ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����Ԫ��R������������Ӧ��ˮ����ķ���ʽ��H2RO4����Ԫ�������ڱ���λ�ڣ� ��
A.IVA��B.VA��C.VIA��D.VIIA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£����и���������ָ����Һ���ܴ����������
A. 0.1 mol��L1��FeCl2��Һ�У�H+��Al3+��SO42����ClO
B. ��ɫ������Һ�У�Al3+��Fe3+��NO3����SCN��
C. ��Al��Ӧ�ܷ�H2����Һ�У�Cu2+��NH4+��CO32-��Cl
D. c(OH)/c(H+)=1��1014����Һ�У�K+��Na+��I��SiO32��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com