�ϳɰ����������Ĵ����������˹��̵���;�����Ի�ѧ��ҵ����Ҳ�������ش�Ӱ�죮�ϳɰ���Ӧ�Ļ�ѧ����ʽΪ��N
2��g��+3H
2��g��

2������NH
3��g����H=-92.2kJ/mol���ϳɰ���ҵ��ԭ����N
2�ɴӿ����з���õ���H
2���ü����ڸ�������ˮ������Ӧ�Ƶã�
��1����һ�ݻ��̶����ܱ�������ע��N
2��H
2�������壬����������Ӧ����ij�¶��´ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�Ϊc��H
2��=9.00mol/L��c��N
2��=3.00mol/L��c��NH
3��=4.00mol/L�����¶��¸÷�Ӧ��ƽ�ⳣ��Ϊ
7.32��10-3
7.32��10-3
��
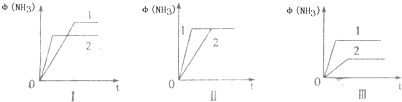
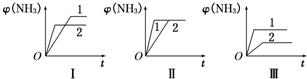
��2��������ͬ�����и�����1molN
2��3molH
2���ڲ�ͬ�����·�Ӧ���ﵽƽ�⣬�������������ʱ��ı仯��ͼ��ʾ������˵����ȷ����
D
D
������ţ���
A��ͼI�����Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��P
2��P
1B��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��P
1��P
2C��ͼ������Dz�ͬ�¶ȶԷ�Ӧ��Ӱ�죬��T
1��T
2D��ͼ��һ������ͬ��ͬѹ�²�ͬ�����Է�Ӧ��Ӱ�죬�Ҵ���Ч��1��2
��3����ˮ����ͨ�����ȵ�̿������ˮ��������ѧ����ʽΪ��C��s��+H
2O��g��
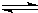
H
2��g��+CO��g����H=+131.3kJ����S=+133.7J/K�÷�Ӧ�ڵ������ܷ��Է�
��
��
����ܻ��
��4�������ڸ�������ˮ������Ӧ��Ӧ����ʽΪ��CH
4��g��+H
2O��g��=CO��g��+3H
2��g�����������ʵ�ȼ�����������±���
| �� �� |
ȼ���ȣ�kJ?mol-1�� |
| H2��g�� |
-285.8 |
| CO��g�� |
-283.0 |
| CH4��g�� |
-890.3 |
��֪1mol H
2O��g��ת��Ϊ1mol H
2O��l��ʱ�ų�44.0kJ������д��CH
4��H
2O�ڸ����·�Ӧ���Ȼ�ѧ����ʽ
CH4��g��+H2O��g��=CO��g��+3H2��g����H=+206.1kJ?mol-1
CH4��g��+H2O��g��=CO��g��+3H2��g����H=+206.1kJ?mol-1
��
��5����������Ѱ����ʵĴ����͵缫���ϣ���N
2��H
2Ϊ�缫��Ӧ���HCl-NH
4ClΪ�������Һ��ȡ����ȼ�ϵ�أ���д���õ�ص�������Ӧʽ
N2+6e-+8H+=2NH4+
N2+6e-+8H+=2NH4+
��




 3NH3��g����H=-92.2kJ/mol���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����ڸ�������ˮ������Ӧ�Ƶã��ҹ��ϳɰ���ҵĿǰ����������Ϊ������-����ý���¶�-400��500�棬ѹǿ-30��50MPa��
3NH3��g����H=-92.2kJ/mol���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����ڸ�������ˮ������Ӧ�Ƶã��ҹ��ϳɰ���ҵĿǰ����������Ϊ������-����ý���¶�-400��500�棬ѹǿ-30��50MPa�� 2������NH3��g����H=-92.2kJ/mol���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����ڸ�������ˮ������Ӧ�Ƶã�
2������NH3��g����H=-92.2kJ/mol���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����ڸ�������ˮ������Ӧ�Ƶã�
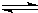 H2��g��+CO��g����H=+131.3kJ����S=+133.7J/K�÷�Ӧ�ڵ������ܷ��Է�
H2��g��+CO��g����H=+131.3kJ����S=+133.7J/K�÷�Ӧ�ڵ������ܷ��Է�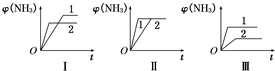 �ϳɰ����������Ĵ����������˹��̵���;�����Ի�ѧ��ҵ����Ҳ�������ش�Ӱ�죮�ϳɰ���Ӧ�Ļ�ѧ����ʽΪN2��g��+3H2��g��?2NH3��g����H=-92.2kJ?mol-1���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����̿��ˮ������Ӧ�Ƶã�
�ϳɰ����������Ĵ����������˹��̵���;�����Ի�ѧ��ҵ����Ҳ�������ش�Ӱ�죮�ϳɰ���Ӧ�Ļ�ѧ����ʽΪN2��g��+3H2��g��?2NH3��g����H=-92.2kJ?mol-1���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����̿��ˮ������Ӧ�Ƶã�