
下列A、B两种元素的原子序数,其中可以组成AB2型离子化合物的是( )
A.6和8 B.19和16 C.12和17 D.10和8
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:问答题
今有甲、乙、丙、丁四种元素。已知:甲元素是自然界中含量最多的元素;乙元素为金属元素,它的原子核外K层、L层电子数之和等于M、N层电子数之和;丙元素的单质及其化合物的焰色反应都显黄色;氢气在丁元素单质中燃烧火焰呈苍白色。
(1)试推断并写出甲、乙、丙、丁四种元素的名称和符号;
(2)写出几种上述元素两两化合形成的化合物的化学式。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关叙述中,不可以用氢键来解释的是
| A.0℃时,水的密度大于冰的密度 | B.水的熔沸点高于硫化氢的熔沸点 |
| C.氟化氢气体极易溶于水 | D.氟化氢比氯化氢稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图所示。已知断裂1mol N-N吸收167kJ热量,生成1 mol N≡N放出942kJ热量,根据以上信息判断,下列说法正确的是
| A.1mol N4转变成N2将放出882kJ热量 | B.N4属于一种新型的化合物 |
| C.N4与N2互为同分异构体 | D.N4是由极性键组成的分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用价电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,也可推测键角大小,下列判断正确的是
| A.CS2是V形分子 | B.SnBr2键角大于120° |
| C.BF3是三角锥形分子 | D.NH4+键角等于109.5° |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有机物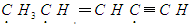 中标有“·”的碳原子的杂化方式依次为
中标有“·”的碳原子的杂化方式依次为
| A.sp、sp2、sp3 | B.sp3、sp2、sp | C.sp2、sp、sp3 | D.sp3、sp、sp2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com