
已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|
|温度/ ℃ |
700 |
900 |
830 |
1000 |
1200 |
|
平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。,则6s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为 ;
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c. c(A)不随时问改变 d.单位时间里生成c和D的物质的量相等
(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为
。
A(g)+B(g)的平衡常数的值为
。
(1) 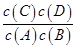 <(2) 0.022 0.09
80% 80% (3)c (4) 2.5
<(2) 0.022 0.09
80% 80% (3)c (4) 2.5
【解析】(1)因反应中的物质都是气体,据平衡常数的定义可知其K=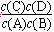 ;由表中数据可知,温度升高,K值减小,说明升高温度向吸热的逆反应方向移动,故正反应为放热反应,即ΔH<0。
;由表中数据可知,温度升高,K值减小,说明升高温度向吸热的逆反应方向移动,故正反应为放热反应,即ΔH<0。
(2)υ(A)=0.003 mol·L-1·s-1 ,则6s后A减少的浓度c(A)= υ(A)t=0.018 mol·L-1,故剩余的A的浓度为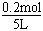 -0.018 mol·L-1=0.022 mol·L-1;A减少的物质的量为0.018 mol·L-1×5L=0.09mol,根据方程式的系数关系,生成的C的物质的量也为0.09mol。
-0.018 mol·L-1=0.022 mol·L-1;A减少的物质的量为0.018 mol·L-1×5L=0.09mol,根据方程式的系数关系,生成的C的物质的量也为0.09mol。
设830℃达平衡时,转化的A的浓度为x,则:
A(g)+B(g)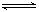 C(g)+D(g)
C(g)+D(g)
起始浓度(mol·L-1) 0.04 0.16 0 0
转化浓度(mol·L-1) x x x x
平衡浓度(mol·L-1) 0.04-x 0.16-x x x
有: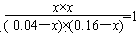 , 解得x =0.032,故A的转化率α(A)=
, 解得x =0.032,故A的转化率α(A)=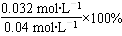 =80%;由于容器的体积是固定的,通入氩气后各组分的浓度不变,反应速率不改变,平衡不移动。
=80%;由于容器的体积是固定的,通入氩气后各组分的浓度不变,反应速率不改变,平衡不移动。
(3)由于该反应是气体分子数不变的反应,容器中压强、气体的密度都永远不变,故a、b错;c(A)随反应的进行要减小,故c可以;不论是否达平衡,单位时间里生成C和D的物质的量永远相等,故d错。
(4)反应“
C(g)+D(g)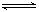 A(g)+B(g)”与“A(g)+B(g)
A(g)+B(g)”与“A(g)+B(g)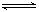 C(g)+D(g)”互为逆反应,平衡常数互为倒数关系,故1200℃时,C(g)+D(g)
C(g)+D(g)”互为逆反应,平衡常数互为倒数关系,故1200℃时,C(g)+D(g)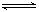 A(g)+B(g)的K==2.5。
A(g)+B(g)的K==2.5。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 绿矾晶体(FeSO4?7H2O)在医药上作补血剂.某同学用KMnO4溶液滴定绿矾晶体(FeSO4?7H2O)样品(杂质不与 KMnO4反应),对铁元素含量进行测定.
绿矾晶体(FeSO4?7H2O)在医药上作补血剂.某同学用KMnO4溶液滴定绿矾晶体(FeSO4?7H2O)样品(杂质不与 KMnO4反应),对铁元素含量进行测定.查看答案和解析>>
科目:高中化学 来源:2014届山西省等四校高三第一次联考化学试卷(解析版) 题型:填空题
已知A(g)+B(g)  2 C(g)反应的平衡常数和温度的关系如下:
2 C(g)反应的平衡常数和温度的关系如下:
|
温度/ ℃ |
700 |
800 |
830 |
1000 |
1200 |
|
平衡常数 |
1.70 |
1.10 |
1.00 |
0.60 |
0.40 |
回答下列问题:
(1) 该反应的平衡常数表达式K=______,△H_____0(填“<”“>”“=”);
(2) 容积固定,判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.气体的密度不随时间改变 b. c(A)不随时间改变
c.混合气体平均相对分子质量不随时间改变 d. 压强不随时间改变
(3)1200℃时反应2C(g)  A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。
(4)830℃时,向一个10.00 L的密闭容器中充入0.40mol的A和1.60mol的B,如果反应初始2s内生成C的物质的量为0.40mol,则2s内A的平均反应速率v(A)= ____mol·L-1·s-1; 2s时c(B)= ____ mol·L-1; 2s时A的转化率为____;2s时C的体积分数为____。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年上海市长宁区高三上学期期末教学质量调研化学试卷(解析版) 题型:填空题
已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|
温度/℃ |
700 |
900 |
830 |
1000 |
1200 |
|
平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
回答下列问题:
(1) 830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1,则6s时c(A)=________mol·L-1, C的物质的量为______ mol;此时,正反应速率_____________(填“大于”、“小于”或“等于”)逆反应速率。
(2)在恒容密闭容器中判断该反应是否达到平衡的依据为________(填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c. c(A)不随时间改变 d.单位时间里生成c和D的物质的量相等
(3)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为___________________。
A(g)+B(g)的平衡常数的值为___________________。
(4)绝热容器不与外界交换能量,在恒容绝热条件下,进行2M(g)+N(g) 2P(g)+Q(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高,简述该反应的平衡常数与温度的变化关系:__________________________________________________________________________________。
2P(g)+Q(s)反应,按下表数据投料,反应达到平衡状态,测得体系压强升高,简述该反应的平衡常数与温度的变化关系:__________________________________________________________________________________。
|
物 质 |
M |
N |
P |
Q |
|
起始投料/mol |
2 |
1 |
2 |
0 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年海南省琼海市高三下学期第一次月考化学试卷(解析版) 题型:填空题
已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|
|温度/ ℃ |
700 |
900 |
830 |
1000 |
1200 |
|
平衡常数 |
1.7 |
1.1 |
1.0 |
0.6 |
0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H 0(填“<”“ >”“ =”);
(2)830℃时,向一个2 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.005 mol·L-1·s-1。,则6s时c(A)= mol·L-1, C的物质的量为 mol;若反应经一段时间后,达到平衡时A的转化率为 ;
(3)判断该反应是否达到平衡的依据为 (填正确选项前的字母):
a.压强不随时间改变 b.c(A)不随时间改变
c.气体的密度不随时间改变 d.单位时间里生成C和D的物质的量相等
(4)1000℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为 。
A(g)+B(g)的平衡常数的值为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com