
【题目】设NA是阿伏加德罗常数的值。下列说法正确的是( )
A.1mol![]() 中共平面的碳原子数最多为6NA
中共平面的碳原子数最多为6NA
B.1L0.5mol/LKHC2O4溶液中含HC2O4-和H2C2O4的数目为0.5NA
C.25℃、1.01×105 Pa下,44.8LSO2和CO2的混合气体中所含分子数为2NA
D.12.0gNaHSO4和MgSO4的固体混合物中所含阳离子总数为0.1NA
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是

A. 图1表示的反应为放热反应
B. 图1中Ⅰ、Ⅱ两点的速率v(Ⅰ)>v(Ⅱ)
C. 图2表示A(?)+2B(g)![]() 2C(g) ΔH<0,达平衡后,在t1、t2、t3、t4时都只改变了一种外界条件的速率变化,由图可推知A不可能为气体
2C(g) ΔH<0,达平衡后,在t1、t2、t3、t4时都只改变了一种外界条件的速率变化,由图可推知A不可能为气体
D. 图3装置的总反应为4Al+3O2+6H2O=4Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了甲烷燃料电池并探究某些工业电解原理(如图所示),其中乙装置为探究氯碱工业原理(X为阳离子交换膜,C为石墨电极),丙装置为探究粗铜精炼原理。请回答下列问题:

(1)从 b口通入的气体发生的电极反应为______________________________。
(2)写出乙中发生的总反应的离子方程式为________________________________。
(3)当b口消耗标况下2.24L的气体时,则A极增重质量为__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g) ![]() 2C(g)+3D(g)在四种不同情况下的反应速率如下,其中表示
2C(g)+3D(g)在四种不同情况下的反应速率如下,其中表示
反应速率最快的是
A. v(A)=0.20mol·L-1·min-1 B. v(B)=0.30 mol·L-1·min-1
C. v(C)=0.40 mol·L-1·min-1 D. v(D)=0.50 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】网络趣味图片“一脸辛酸”,是在人脸上重复画满了辛酸的键线式结构。下列有关辛酸的叙述正确的是

A. 辛酸的羧酸类同分异构体中,含有三个“-CH3”结构,且存在乙基支链的共有7种
B. 辛酸的同分异构体(CH3)3CCH(CH3)CH2COOH的名称为2,2,3一三甲基戊酸
C. 正辛酸常温下呈液态而软脂酸常温下呈固态,故二者不符合同一通式
D. 辛酸的同分异构体中能水解生成相对分子质量为74的有机物的共有8种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白色固体混合物A,含有KCl、CaCO3、Na2CO3、Na2SiO3、CuSO4中的几种,常温常压下进行如下实验。

下列推断不正确的是
A. 无色溶液B的pH≥7
B. 白色固体F的主要成分是H2SiO3
C. 混合物A中有Na2SiO3、CuSO4和CaCO3
D. 在无色溶液B中加HNO3酸化,无沉淀;再滴加AgNO3,若有白色沉淀生成,说明混合物A中有KCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对甲基苯乙烯(![]() )是有机合成的重要原料。下列对其结构与性质的推错误的是( )
)是有机合成的重要原料。下列对其结构与性质的推错误的是( )
A. 分子式为![]()
B. 能发生加聚反应和氧化反应
C. 具有相同官能团的芳香烃同分异构体有5种![]() 不考虑立体异构
不考虑立体异构![]()
D. 分子中所有原子可能处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O3·5H2O可作为高效脱氯剂,工业上用硫铁矿(FeS2)为原料制备该物质的流程如下。
![]()
已知:I.气体A可以使品红溶液褪色,与硫化氢(H2S)混合能获得单质硫。
Ⅱ.pH约为11的条件下,单质硫与亚硫酸盐可以共热生成硫代硫酸盐。
回答下列问题:
(1)沸腾炉中将粉碎的硫铁矿用空气吹动使之达到“沸腾”状态,其目的是______________。
(2)吸收塔中的原料B可以选用_____________(填字母序号)。
A.NaCl溶液 B.Na2CO3溶液 C.Na2SO4溶液
(3)某小组同学用下图装置模拟制备Na2S2O3的过程(加热装置已略去)。
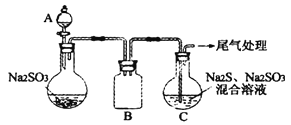
①A中使用70%的硫酸比用98%的浓硫酸反应速率快,其原因是_____________。装置B的作用是______________。
②C中制备Na2S2O3发生的连续反应有:Na2S+H2O+SO2=Na2SO3+H2S_____________和Na2SO3+S![]() Na2S2O3 。
Na2S2O3 。
(4)工程师设计了从硫铁矿获得单质硫的工艺,将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,该反应的化学方程式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com