
| A.H2O2>S O2>SO2 | B.H2O2>O2 Br2>O2 |
| C.Br2>H2O2 SO2>S | D.Br2>H2O2 Br2>SO2 |
 能力评价系列答案
能力评价系列答案科目:高中化学 来源:不详 题型:填空题
 ①
①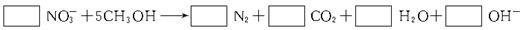
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NF3是氧化剂,H2O是还原剂 |
| B.还原剂与氧化剂的物质的量之比为2:1 |
| C.若生成0.2 mol HNO3,则转移0.2 mol电子 |
| D.NF3在潮湿的空气中泄漏会产生红棕色气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Si+2CO↑,下列说法正确的是
Si+2CO↑,下列说法正确的是| A.SiO2是氧化剂 | B.SiO2发生氧化反应 |
| C.C表现出氧化性 | D.C被还原 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CuSO4+SO2↑+2H2O,对于该反应,下列说法中不正确的是
CuSO4+SO2↑+2H2O,对于该反应,下列说法中不正确的是| A.是氧化还原反应 | B.浓硫酸是还原剂 |
| C.H2SO4表现了氧化性和酸性 | D.反应中Cu发生了氧化反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4…… |
| ② | C12、FeBr2 | FeC13、FeBr3 |
| ③ | MnO4-…… | C12、Mn2+…… |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.氧化性:KClO3>H3PO4 | B.氧化性:H3PO4>KClO3 |
| C.还原性:PH3>X | D.还原性:X>PH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氧化性Cr2O72->Fe3+>SO2 |
| B.Cr2O72-能将Na2SO3氧化成Na2SO4 |
| C.每有1 mol K2Cr2O7参加反应,转移电子的数目为3NA |
| D.若6.72 L SO2(标准状况)参加反应,则最终消耗0.1 mol K2Cr2O7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com