
【题目】设NA为阿伏加德罗常数的数值,下列说法错误的是( )
A.一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA
B.256g S8分子中含S﹣S键为7NA个 
C.由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO﹣数目为NA个
D.1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个
【答案】B
【解析】解:A.一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后,该反应为气体体积减小的可逆反应,所以反应后气体的物质的量大于2mol,反应后容器中的分子数大于2NA , 故A正确;
B.256g S8晶体含有S8的物质的量为1mol,1molS8中含有8mol S﹣S键,含有的S﹣S键为8NA个,故B错误;
C.由1mol CH3COONa和少量CH3COOH形成的中性溶液中,含有1mol钠离子;根据电荷守恒,溶液为中性,氢离子与氢氧根离子物质的量相等,则钠离子与CH3COO﹣的物质的量相等,所以溶液中含有CH3COO﹣的物质的量为1mol,含有的CH3COO﹣数目为NA个,故C正确;
D.1molNa完全反应失去1mol电子,无论产物为氧化钠还是过氧化钠,转移的电子数都为1mol,转移电子总数NA个,故D正确;
故选B.


科目:高中化学 来源: 题型:
【题目】在与外界隔离的体系中,自发过程将导致体系的熵 , (填“增大”、“减小”、“不变”);对于同一种物质,时熵值最大.(填“固态”、“液态”、“气态”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1molN﹣N吸收193kJ热量,生成1molN≡N放出941kJ热量.根据以上信息和数据,下列说法正确的是( ) 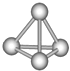
A.N4属于一种新型的化合物
B.N4是N2的同系物
C.N4转变为N2 是物理变化
D.1molN4气体转变为N2放出724kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按以下步骤可从![]() 合成
合成![]() (部分试剂和反应条件已略去)
(部分试剂和反应条件已略去)

请回答下列问题:
(1)分别写出B、D的结构简式:
B.__________________________________,
D.__________________________________;
(2)反应①~⑦中属于消去反应的是_____________。(填反应代号)
(3)如果不考虑⑥⑦反应,对于反应⑤,得到E的可能的结构简式为_____________________。
(4)试写出C→D反应的化学方程式_____________________________
(有机物写结构简式,并注明反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠及其化合物具有广泛的用途.
(1)工业上制备金属钠的常用方法是 . 试写出制备金属钠的化学方程式 . 金属钠可用于 (写出Na在熔点低方面的一种用途).
(2)用Na2CO3熔融盐作电解质,CO、O2、CO2为原料可组成新型电池.该电池的结构如图所示:
①正极的电极反应式为 , 电池工作时物质A可循环使用,A物质的化学式为 .
②请写出检验Na2CO3中钠元素的方法 .
(3)常温下,浓度均为0.1molL﹣1的下列五种钠盐溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaCO | NaCN |
pH | 8.8 | 9.7 | .6 | 0.3 | . |
上述盐溶液的阴离子中,结合H+能力最强的是 , 根据表中数据,浓度均为0.01molL﹣1的下列四种酸的溶液分别稀释100倍,pH变化最大的是(填序号).
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯.
①常温下,当300mL 1molL﹣1的NaOH溶液吸收4.48L(折算成标准状况)SO2时,所得溶液pH>7,则溶液中各离子浓度由大到小的顺序为 .
②已知几种离子开始沉淀时的pH如下表:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加某浓度的NaOH溶液时,(填离子符号)先沉淀,Ksp[Fe(OH)2] Ksp[Mg(OH)2](填“>”、“=”或“<”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在A、B、C三个烧杯中分别盛有相同浓度的稀硫酸,如图所示:
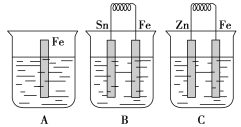
(1)A中反应的离子方程式为_____________________________。
(2)B中Sn极的电极反应式为____________________________,Sn极附近溶液的pH________(填“增大”、“减小”或“不变”)。C中被腐蚀的金属是________,总反应的离子方程式为________________,比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】韩国三星公司因为手机电池爆炸而屡屡曝光,电池的安全性和环保性再次被公众所重视。一种以引火性高的联氨(N2H4)为燃料的环保电池,工作时产生稳定无污染的物质,原理如图所示。下列说法正确的是

A.N极为电源负极,联氨从c口通入
B.负极上每消耗l mol N2H4,转移6 mol电子
C.正极的电极反应式为:O2+2H2O+4e=4OH
D.可将联氨改进为引火性低、稳定性好的N2H4·H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com