
����Ŀ����ͼ�У�AΪһ����ѧ��ѧ�г����ĵ��ʣ�B��C��D��E�Ǻ���AԪ�صij�����������ǵ���ɫ��Ӧ��Ϊ��ɫ��
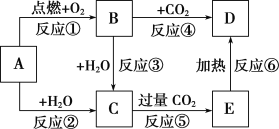
(1)����6����Ӧ������������ԭ��Ӧ����________(��д���)��
(2)B��������������Ŀ��Ϊ________��
(3)д��A��C��Ӧ�Ļ�ѧ����ʽ__________________________________��
(4)д��B��C��Ӧ�����ӷ���ʽ��________________________________��
(5)д��C��E��Ӧ�����ӷ���ʽ��________________________________��
(6)����5.00 g D��E�Ĺ������ʹE��ȫ�ֽ⣬�������������������0.62 g����ԭ�������D����������Ϊ_________��
���𰸡��٢ڢۢ� 1��2 2Na+2H2O��2NaOH+H2�� 2Na2O2��2H2O��4Na����4OH����O2�� OH�� + CO2��HCO3- 66.4%
��������
A��B��C��D��E����ɫ��ӦΪ��ɫ��˵����������Ԫ�أ�AΪ���ʣ���AΪNa������ת����ϵ���Ƴ�BΪNa2O2��CΪNaOH��DΪNa2CO3��EΪNaHCO3���ݴ˷�����
��1����Ӧ����Na��O2��Ӧ��2Na��O2 ![]() Na2O2������������ԭ��Ӧ����Ӧ��Ϊ2Na��2H2O=2NaOH��H2��������������ԭ��Ӧ����Ӧ��2Na2O2��2H2O=4NaOH��O2��������������ԭ��Ӧ����Ӧ��Ϊ2Na2O2��2CO2=2Na2CO3��O2��������������ԭ��Ӧ����Ӧ��NaOH��CO2=NaHCO3��������������ԭ��Ӧ����Ӧ����2NaHCO3
Na2O2������������ԭ��Ӧ����Ӧ��Ϊ2Na��2H2O=2NaOH��H2��������������ԭ��Ӧ����Ӧ��2Na2O2��2H2O=4NaOH��O2��������������ԭ��Ӧ����Ӧ��Ϊ2Na2O2��2CO2=2Na2CO3��O2��������������ԭ��Ӧ����Ӧ��NaOH��CO2=NaHCO3��������������ԭ��Ӧ����Ӧ����2NaHCO3 ![]() Na2CO3��CO2����H2O��������������ԭ��Ӧ��
Na2CO3��CO2����H2O��������������ԭ��Ӧ��
��2����������������BΪ�������ƣ������ʽΪ![]() ���������Ӹ�����Ϊ1��2��
���������Ӹ�����Ϊ1��2��
��3������(1)�ķ�������Ӧ�ڵĻ�ѧ����ʽΪ2Na��2H2O=2NaOH��H2����
��4������(1)�ķ�������Ӧ�۵����ӷ���ʽΪ2Na2O2��2H2O=4Na����4OH����O2����
��5����Ӧ�ݵ����ӷ���ʽΪOH����CO2=HCO3����
��6����������������DΪNa2CO3��EΪNaHCO3�����ȸû�������2NaHCO3 ![]() Na2CO3��CO2����H2O�����У�
Na2CO3��CO2����H2O������
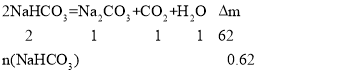
���n(NaHCO3)=0.02mol����Na2CO3��������Ϊ![]() ��100%=66.4%��
��100%=66.4%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ء��������dz������ǹ���ѩ���ʳƷ����ɫ������Ҫ�ɷ֣��ṹ��ͼ��ʾ��
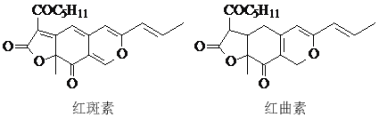
����˵����ȷ���ǣ� ��
A.����غͺ����ػ�Ϊͬ���칹��
B.����غͺ����ض�����NaOH��Һ��Ӧ
C.������к����Ѽ����ʻ������ֺ���������
D.�������������6molH2�ӳ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���õ��з�̪���Ȼ�����Һʪ�����ֽ�ֱ����ס�������ʵ�飬�����жϴ�����ǣ� ��

A.b������������ð��B.d���������ֺ�ɫ
C.a��c���϶�����������ӦD.����������������������ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ʊ�пӡˢ��·������ϡ���ḯʴп������ķ�Һ�����ð�Һ�������ð�Һ���г�������п�⣬����������ˮ�����Cl����Fe3+����ʵ����������ð�Һ��ȡZnSO47HO�Ĺ�����ͼ��ʾ
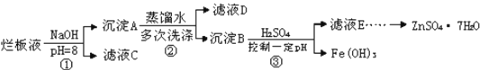
��1����ϡ���ḯʴп��ʱ��ԭ����ΪN2O���������뻹ԭ�������ʵ���֮����_________
��2��������ٵ�pH��12����Zn(OH) 2�ܽ�����ƫп���ƣ�Zn(OH) 2�ܽ�����ӷ���ʽΪ___________________________
��3����ҺD�г��˺���OH�������⣬�����е���������___________�������ӷ��ţ�
��4������ҺE��pH��4��c��Zn2������2mol��L-1,��Fe3������2.6��10-9mo��L-l�����Fe��OH��3���ܶȻ�����________________��ֻд�����
��5����֪:��Fe��OH��3��s�� Fe3����aq����3OH����aq��H��a kJ mol��L-1
��H2O(l) H����aq����OH����aq��H��b kJ��mol��L-1
���ٵ��ܶȻ�����ΪKsp���ڵ����ӻ�����ΪKw��Fe3������ˮ�ⷴӦ��ƽ�ⳣ��:K��______________���ú�Kw��Ksp�Ĵ���ʽ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������㶨Ϊ2L���ܱ����������2mol M��һ������N���������·�Ӧ��M��g��+ N��g��![]() E��g��������Ӧ���е�4minʱ�ﵽƽ�⣬��֪M��Ũ��Ϊ0.2molL-1������˵����ȷ���ǣ� ��
E��g��������Ӧ���е�4minʱ�ﵽƽ�⣬��֪M��Ũ��Ϊ0.2molL-1������˵����ȷ���ǣ� ��
A. 4minʱ��M��ת����Ϊ80%
B. 4minʱ����M��ʾ�ķ�Ӧ����Ϊ0.8molL-1min-1
C. 4min���������г��벻���뷴Ӧ��ϡ�����壬M�����ʵ�����С
D. 2minʱ��M�����ʵ���Ũ��Ϊ0.6molL-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ����������ԭ��Ӧ���ǣ�������
A. SO3+ H2O= H2SO4 B. NH4Cl ![]() NH3
NH3![]() +HCl
+HCl![]()
C. Fe+CuSO4= FeSO4+Cu D. NaOH+HNO3=NaNO3+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС�鱨�ú�ϡ�����KMnO4����Һ��H2C2O4��Һ�����ᣩ�ķ�Ӧ���˷�ӦΪ���ȷ�Ӧ����̽���������Ի�ѧ��Ӧ���ʵ�Ӱ�죢�������������ķ�����¼ʵ������������Һ�������仯������ѡ�Լ�������:0.2mol L-1H2C2O4��Һ��0.010mol��L-1KMnO4��Һ�����ԣ�������ˮ���Թܡ���Ͳ�����������ˮԡ��
��Ŀ | V(0.2mol L-1H2C2O4��Һ��/mL | V(����ˮ��/mL | V(0.010mol��L-1KMnO4��Һ��/mL | M(MnSO4���壩/g | T/�� | �� |
�� | 2.0 | 0 | 4.0 | 0 | 50 | |
�� | 2.0 | 0 | 4.0 | 0 | 25 | |
�� | 1.0 | a | 4.0 | 0 | 25 | |
�� | 2.0 | 0 | 4.0 | 0.1 | 25 |
�ش���������
��1���������Ӧԭ���Ļ�ѧ��Ӧ����ʽ____________________________________
��2������ʵ��٢���̽��___________�Ի�ѧ��Ӧ���ʵ�Ӱ�죻������ʵ��ڢ���̽��Ũ�ȵĶԻ�ѧ��Ӧ���ʵ�Ӱ�죬��aΪ______������ʵ����Ҫ���������������������������Ӧ��д_______������ʵ��ڢ���̽��__________�Ի�ѧ��Ӧ���ʵ�Ӱ��
��3����֪����Ϊ��Ԫ���ᣬ����뷽��ʽΪ___________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п�̸ɵ�صĸ��������ǵ�ؿ���Ľ���п�������DZ��������̺�̼�۰�Χ��ʯī�缫����������Ȼ�п���Ȼ�淋ĺ�״��õ�طŵ�����в���Mn2O3�����÷Ͼɵ�ػ���Zn��Mn������Ի������������ش�
����һ�����ȥ���弰ʯī�缫�ĺ�ɫ��״���м�ˮ�����裬����ܽ⣬�����˷���õ��������Һ��
��������������壬��ȡMnO2ͨ���Ի�õ������������գ����յ�Ŀ����__������ʱ�õ���ʵ�������оƾ��ơ���������__��
��������������Һ���õ�ZnCl2��xH2O���壬��ͨ����SOCl2��ZnCl2��xH2O�����Ͽ���ȡ��ˮZnCl2���йص�ʵ��װ����ͼ���гּ�����װ���ԣ���
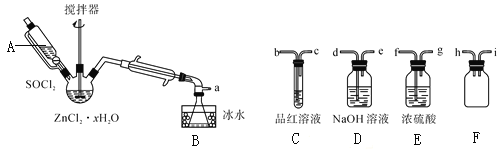
��֪��SOCl2��һ�ֳ��õ���ˮ�����۵�-105�����е�79����140�������ֽ⣬��ˮ���ҷ�Ӧ�����������塣
������A������Ϊ__��
��������ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ��__��
��Ϊ����ʣ���SOCl2����֤�������к���SO2������������Ŀ����������Ϊa��__��װ��E��Ũ���������___��
��Ϊ���SOCl2�������ʣ���ʵ���˲��õļ��ȷ�ʽΪ__��
�����ۣ���ZnCl2��xH2O�������������м��Ⱦ��գ�__���ܣ����ܣ��õ���ˮZnCl2��ԭ����__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl3��Һ������ʴ�̵�·�壬ʴ�̺��������Һ�к���Cu2����Fe2����Fe3����Cl���ȡ����и����������ڸ�������Һ�д���������ǣ�������
A.Na����Al3����Cl����SO42-B.Ca2����Mg2����NO3-��ClO��
C.K����NH![]() ��SO32-��AlO2-D.Ba2����K����I����NO3-
��SO32-��AlO2-D.Ba2����K����I����NO3-
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com