
【题目】判断下列物质按碱性减弱、酸性增强的顺序依次排列正确的是
A.厨房清洁剂 肥皂 醋 厕所清洁剂
B.醋 厕所清洁剂 肥皂 厨房清洁剂
C.厕所清洁剂 醋 肥皂 厨房清洁剂
D.厨房清洁剂 厕所清洁剂 醋 肥皂
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:
【题目】在下列溶液中的物质的量浓度最大的是
A.0.5L 0.1mol/L的NaCl溶液 B.100mL 0.2mol/L的MgCl2溶液
C.1L 0.2mol/L的AlCl3溶液 D.1L 0.3mol/L盐酸溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含氮污染物的治理是环保的一项重要工作。合理应用和处理氮的化合物,在生产生活中有重要意义。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJmol﹣1
2C(s)+O2(g)=2CO(g) △H=﹣221.0kJmol﹣1
C(s)+O2(g)=CO2(g) △H=﹣393. 5kJmol﹣1
则汽车尾气处理的反应之一:2NO(g)+2CO(g)=N2(g)+2CO2(g)△H=_____ kJmol﹣1,利于
该反应自发进行的条件是_______(选填“高温”或“低温”)。

(2)将0.20mol NO和0.10molCO充入一个容积恒定为1L的密闭容器中发生反应:
2NO(g)+2CO(g)N2(g)+2CO2(g),反应过程中 部分物质的浓度变化如图所示:
反应从开始到9min时,用CO2表示该反应的速率是____________________(保留2位有效数字)
②第12min时改变的条件是______________(填“升温或降温”).
③第18min时建立新的平衡,此温度下的平衡常数为______________(列计算式),第24min时,若保持温度不变,再向容器中充入CO和N2各0.060mol,平衡将_____移动(填“正向”、“逆向”或“不”)。
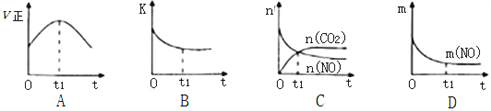
(3)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在t1时刻达到平衡状态的是________________(填序号)。
(如图中v正、K、n、m分别表示正反应速率、平衡常数、物质的量和质量)
(4)以氨为燃料可以设计制造氨燃料电池,产物无污染。若电极材料均为惰性电极,KOH溶液作电解质溶液,则该电池负极电极反应式为______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知煤油的密度是0.8gcm﹣3 , 试根据金属钠的保存方法和金属钠与水反应的现象推断金属钠的密度( )
A.小于0.8 gcm﹣3
B.大于1.0 gcm﹣3
C.介于0.8~1.0 gcm﹣3
D.无法推测
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.NH3溶于水溶液能导电,所以NH3是电解质
B.钢铁发生析氢腐蚀时,负极反应是Fe-3e-=Fe3+
C.等量的氢气和氧气分别完全燃烧生成气态水和液态水,前者放出的热量多
D.H2(g)+F2(g)===2HF(g) ΔH=-271 kJ·mol-1,ΔS=+8 J·mol-1·K-1,该反应在任意温度下都能自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是
A. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
B. 核外电子排布相同的微粒化学性质也相同
C. Cl-、S2、Ca2+、K+半径逐渐减小
D. ![]() Cl与
Cl与![]() Cl得电子能力相同
Cl得电子能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2与O2、F2均能发生反应,下图为H2与F2发生反应生成HF过程中的能量变化示意图。请回答
下列问题:
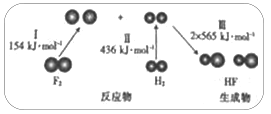
H2(g)与F2(g)反应生成HF(g)过程中的能量最变化
(1)完成转化I、II_________(填“吸收”或“放出”,下同)能量,完成转化Ⅲ_________能量。
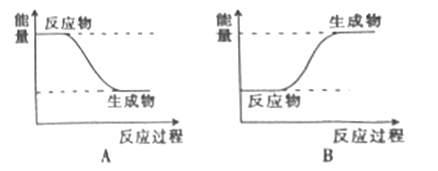
(2)H2和F2反应的能量变化图可用___________(填“A”或“B”)表示。
(3)H2在O2中燃烧的过程主要是__________能转化为_______能的过程。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将HI(g)置于密闭容器中,某温度下发生下列变化:2HI(g) ![]() H2(g)+I2(g)△H<0
H2(g)+I2(g)△H<0
(1)该反应平衡常数的表达式为K=______________,则H2(g)+I2(g) ![]() 2HI(g)平衡常数的表达式为K1=_____________(用K表示)。
2HI(g)平衡常数的表达式为K1=_____________(用K表示)。
(2)当反应达到平衡时c(I2)=0.5mol/L,c(HI)=4mol/L,则c(H2)为________,HI的分解率为________。
(3)能判断该反应达到平衡状态的依据是________
A.容器中压强不变
B.混合气体中c(HI)不变
C.c(I2)=c(H2)
D.v(HI)正=v(H2)逆
(4)若该反应800℃时达到平衡状态,且平衡常数为1.0,某时刻,测得容器内各物质的浓度分别为c(HI)=2.0mol/L,c(I2)=1.0mol/L,c(H2)=1.0mol/L,则该时刻,反应向_________(填“正向”或“逆向”,下同)进行,若升高温度,反应向_________进行。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com