
【题目】TMB是一种新型指纹检测的色原试剂,由碳、氢、氮三种元素组成,M=240g/mol。某研究性学习小组的同学欲利用下列仪器测定TMB的分子式。主要过程为在足量氧气流中将4.80 g TMB样品氧化(氮元素转化为N2),再利用吸收剂分别吸收水蒸气和CO2。请从图中选择适当的装置(装置符合气密性要求,加热装置等已略去,其他用品可自选)。
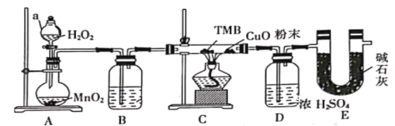
(1)写出仪器a的名称__________,A中的化学反应方程式:___________;
(2)B中试剂是___________,作用是________________ ;
(3)装置C中CuO粉末的作用为________________。
(4)理想状态下,将4.80 gTMB样品完全氧化,点燃C处酒精灯,实验结束时测得D增加3.60 g,E增加14.08 g,则TMB的分子式为____________。
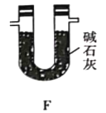
(5)有同学认为,用该实验装置测得的TMB分子式不准确,应在干燥管E后再添加一个装有碱石灰的干燥管F。你认为是否需要添加F装置__________(填“需要”或“不需要”),简述理由________________。
【答案】分液漏斗 ![]() 浓硫酸 干燥 O2,防止将水蒸气带入 D或E 中引起增重 使TMB不充分燃烧生成CO全部转化为CO2 C16H20N2 需要 防止外界空气中的 CO2 和 H2O 进入 E 中,避免对 E 处吸收二氧化碳的定量检测造成干扰
浓硫酸 干燥 O2,防止将水蒸气带入 D或E 中引起增重 使TMB不充分燃烧生成CO全部转化为CO2 C16H20N2 需要 防止外界空气中的 CO2 和 H2O 进入 E 中,避免对 E 处吸收二氧化碳的定量检测造成干扰
【解析】
由实验装置可知,A中过氧化氢在二氧化锰催化作用下生成氧气,B中浓硫酸干燥氧气,C中氧气将TMB氧化为二氧化碳、水和氮气,D中浓硫酸增重为水的质量,E中增重为二氧化碳的质量,结合质量及物质的量计算TMB分子中碳、氢、氮的原子个数比,根据相对分子质量之比算出相对分子质量,结合原子个数比计算出分子式,有必要在干燥管E后再添加一个装有碱石灰的干燥管F,防止空气中的水和二氧化碳进入E,以此解答该题。
(1)由装置图可知,仪器a为分液漏斗, A中发生H2O2在MnO2催化下分解制备氧气,故化学反应方程式为![]() ,故答案为:分液漏斗;
,故答案为:分液漏斗;![]() ;
;
(2)B 中试剂是浓硫酸,作用是干燥O2,防止带入 D或E 中引起增重,故答案为:浓硫酸;干燥O2,防止将水蒸气带入 D或E 中引起增重;
(3)装置C中CuO粉末的作用为使TMB不充分燃烧生成的CO全部转为CO2,故答案为:使TMB不充分燃烧生成CO全部转化为CO2;
(4)实验后称得D、E装置分别增加3.60g、14.08g,则m(H2O)=3.60g,m(CO2)=14.08g,则![]() ,n(H)=2n(H2O)=0.4mol;
,n(H)=2n(H2O)=0.4mol;![]() ,n(C)=n(CO2)=0.32mol;
,n(C)=n(CO2)=0.32mol;
所以![]() ;
;
则:n(C):n(H):n(N)=0.32mol:0.4mol:0.04mol=8:10:1,
TMB的相对分子质量为240,设分子式为C8nH10nNn,则有12×8n+10n+14n=240,解得n=2,所以分子式为C16H20N2,故答案为:C16H20N2;
(5)本实验是通过TMB完全燃烧,并利用D、E装置分别吸收H2O和CO2来确定其分子组成,若不添加F装置,外界空气中的CO2和H2O进入E中,从而干扰 E处吸收二氧化碳的定量检测,给实验造成误差,故答案为:需要;防止外界空气中的CO2和H2O进入E 中,避免对 E 处吸收二氧化碳的定量检测造成干扰。


科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法不正确的是
A.糖类、油脂、蛋白质都能发生水解反应
B.酸性![]() 溶液可以鉴别苯、乙醇和乙酸
溶液可以鉴别苯、乙醇和乙酸
C.苯和乙烯均可以使溴水褪色,但褪色原理不同
D.分子式为![]() 的同分异构体共有4种(不考虑立体异构)
的同分异构体共有4种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰钢是工业上非常重要的一 种合金, 其主要成分锰是用软锰矿(主要成分为MnO2,还含有少量Al2O3、MgO、SiO2)为原料制备的,某种生产工艺流程如下图所示 :
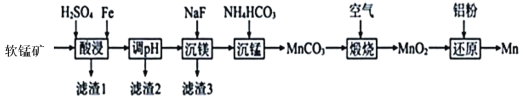
已知:MnO2不溶于稀硫酸,但它可以在酸性条件下和一些还原剂反应生成 Mn2+。
难溶物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 | Mn(OH)2 |
溶度积常数 | 4.0×10-38 | 1.0×10-33 | 1.8×10-11 | 1.8×10-13 |
(1)为了提高锰的浸出率 ,通常需要将软锰矿_______; 酸浸时 MnO2 溶解的离子反应方程式是____________________。
(2)滤渣 2 的主要成分是____________(填化学式)。
(3)沉锰时发生的主要离子反应方程式是________; 沉锰后需要对所得的沉淀进行过滤、洗涤操作,如何检验沉淀己洗净?________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(HOOC-COOH)是一种常见的有机酸,利用淀粉制备草酸的实验流程如图:
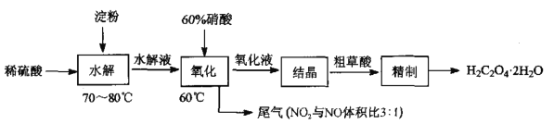
回答下列问题:
(1)“水解”时,检验淀粉是否水解完全,所用的试剂是____;“水解”及“氧化”步骤中适宜的加热方式是________________。
(2)“氧化”时实验装置如图所示(夹持及加热装置已略):
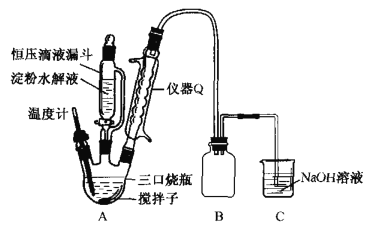
①仪器Q的名称是________.
②三口烧瓶中生成H2C2O4· 2H2O的化学方程式为____________。
③装置B的作用是___________,装置C的作用是_______________。
(3)已知在20℃、70℃时,草酸的溶解度依次为为9. 5 g/(l00g水),84.5g/(l00g水),则粗草酸“精制”需采用的提纯方法为___________________。
(4)探究H2C2O4的性质:
①向NaHCO3溶液中加入草酸溶液,产生大量气体,可得出草酸的酸性比碳酸_____(填“强”或“弱”)。
②向草酸中加入足量C2H5OH和适量浓硫酸加热,产生有芳香气味的油状物。该生成物为___________(写结构简式)。
③向K2Cr2O7溶液中加入H2C2 O4·2H2O析出K[Cr(C2O4)2(H2O)2]晶体,该反应的化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法正确的是
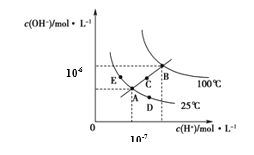
A.图中五点KW间的关系:B>C>A=D=E
B.若从A点到C点,可采用温度不变时在水中加入适量H2SO4 的方法
C.若从A点到D点,可采用在水中加入少量NaOH的方法
D.若处在B点温度时,将pH=2的硫酸与pH=12的KOH等体积混合后,溶液显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列说法正确的是
A.0. 1 mol L-1的CaCl2 溶液中Ca2+的数目为0. lNA
B.标准状况 下,11. 2 L CHCl3 所含的分子数目为0. 5 NA
C.2. 8 g 乙烯含有的共用电子对的数目为 0. 6 NA
D.常温下,1 molFe与足量浓H2SO4反应,转移电子数为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法制备磷酸二氢钾(KH2PO4)装置如图所示。下列说法正确的是
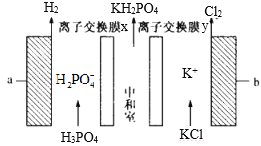
A.与 a 相连接的电源电势比 b 的高
B.离子交换膜 x、y 分别为阳离 子、阴离子交换膜
C.电解时,理论上相同时间内通过交换膜的阴、阳离子数相等
D.当外电路中通过 1mol 电子时,会有ll.2L的Cl2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物A、B、C互为同分异构体,分子式为C5H8O2,有关的转化关系如下图所示,已知A的碳链无支链,且1molA能与4molAg[(NH3)2]OH完全反应;B为五元环酯。
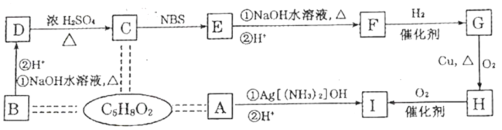
提示:CH3—CH=CH—R![]() Br—CH2—CH=CH—R
Br—CH2—CH=CH—R
(1)A中所含官能团是_____________。A与新制氢氧化铜悬浊液反应的方程式_________________________________。
(2)B、H的结构简式分别为_____________。
(3)写出下列反应方程式(有机化合物用结构简式表示)。
D→C:_____________________________________________________________。
E→F(只写①条件下的反应):_________________________________________。
(4)F的加聚产物的结构简式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,在不同金属离子存在下,过氧化氢经过24h的分解率如下表所示:
离子 | 加入量(mg·L-1) | 分解率/% | 离子 | 加入量(mg·L-1) | 分解率/% |
无 |
| 2 | Fe2+ | 1.0 | 15 |
Al3+ | 10 | 2 | Cu2+ | 0.1 | 86 |
Zn2+ | 10 | 10 | Cr3+ | 0.1 | 96 |
下列有关说法正确的是
A.能使过氧化氢分解反应活化能降低最多的离子是Al3+
B.催化剂可以使平衡移动,提高过氧化氢的分解率
C.若向过氧化氢中加入水,过氧化氢的分解速率加快
D.用等量H2O2制O2时,与自身分解相比,加入足量酸性KMnO4溶液可得到更多O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com