
【题目】亚氯酸钠(NaClO2)是一种高效氧化剂和漂白剂,主要用于棉纺、纸浆漂白和鱼药的制造。制备亚氯酸钠的工艺流程如下:

(1)要加快步骤①的反应速率,可采取的措施为 。(写一种即可)
(2)步骤①的离子方程式为 ,每生成标准状况下22.4L的ClO2,转移电子数为 。
(3)步骤②中H2O2的作用是 ;从“反应混合液”到“产品”的过程中先需蒸发溶剂,写出蒸发所需的硅酸盐仪器的名称 。
(4)NaClO2产品中通常混有少量NaCl。取样品wg,测得Na的物质的量为nmol,则该样品中NaClO2的物质的量为______mol。
【答案】(1)升高温度(或其它合理答案)(2分)
(2)2ClO3-+SO2=2ClO2+SO42- NA
(3)还原剂 酒精灯,蒸发皿,玻璃棒
(4)(w-58.5n)/32
【解析】
试题分析:在酸性条件下NaClO3与SO2发生反应①:2NaClO3+SO2=2ClO2+Na2SO4。母液中主要含有Na2SO4;ClO2气体与 H2O2、NaOH发生反应②:H2O2+2ClO2+2NaOH=2NaClO2+2H2O+O2。因为亚氯酸钠受热易分解,而物质的沸点随压强的增大而升高。所以采用低温、减压法蒸发溶剂,就会得到亚氯酸钠晶体。
(1)要加快步骤①的反应速率,可采取的措施有适当升高反应温度,增大吸收液浓度,增大SO2与吸收液的接触面积,通入更多的SO2等。
(2)反应①的离子方程式是2ClO3-+SO2=2ClO2+SO42-。标准状况下22.4L的ClO2的物质的量是1mol,反应中氯元素化合价从+5价降低到+4价,得到1个电子,则转移电子数为NA;
(3)反应②的方程式为 H2O2+2ClO2+2NaOH=2NaClO2+2H2O+O2,在反应中ClO2把H2O2氧化为O2,它本身被还原为NaClO2。因此该反应的的氧化剂是ClO2,双氧水是还原剂;蒸发所需的硅酸盐仪器有酒精灯,蒸发皿,玻璃棒;
(4)设样品中NaClO2的物质的量为xmol,氯化钠是ymol,则根据钠原子守恒可知x+y=n,根据质量守恒可知90.5x+58.5y=w,解得x=(w-58.5n)/32。


科目:高中化学 来源: 题型:
【题目】A是一种常见的气态烃,其中C、H元素质量比为6:1,其标准状况下的密度为1.25gL-1。B、C、D都是含有C、H、O三种元素的有机物,其中D是一种常见厨房调味品中的主要成分。A、B、C、D间有如下转化关系:

请回答下列问题:
(1)D物质中的官能团 。(写名称)
(2)A→B的反应类型 。
(3)B→C的反应方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电能,其中放电过程为2Li+Cu2O+H2O==2Cu+2Li++2OH-,下列说法不正确的是

A.放电时,Li+透过固体电解质向Cu极移动
B.放电时,正极的电极反应式为O2+2H2O+4e-==4OH-
C.通空气时,铜被腐蚀,表面产生Cu2O
D.整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物。室温为非活性物质。温度升高后变得活泼。在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制造硫酸:

回答下列问题:
(1)在FeS2中的S2-的核外电子排布式是________________________;
(2)常温下Fe3+比Fe2+要更加稳定的原因是__________________________________;
(3)将FeS2与稀盐酸反应得到H2S2,H2S2分子中,共价键的类型是___________________;FeS2氧化得到SO2,在SO2分子中的S原子的杂化轨道类型是______________________ ,写出两个与SO2互为等电子体的分子或离子_______________________。-
(4)H2SO4和H2SO3都是S的含氧酸,请用结构知识解释H2SO4比H2SO3酸性强的原因:
_____________________________________________________________________。
(5)FeS2的晶体中的Fe2+离子的排列方式如下图。
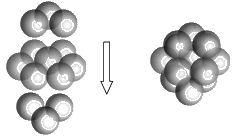
①每个Fe2+周围最近的等距离的S22-离子有____________个。
②已知FeS2的晶胞参数是a0=0.54nm,它的密度为_____________________g·cm-3(列式并计算,阿伏加德罗常数为6.02×1023)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯(![]() )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
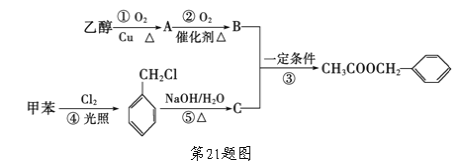
(1)C的结构简式为_______________,B中含氧官能团的名称是____________。
(2)实验室A的方法是:__________________________________________
______________________________________________________________。
(3)写出反应①、⑤的化学方程式:
① ________________________________________;
⑤ ________________________________________。
(4)反应③、④的反应类型分别为③____________、④____________。
(5)反应____(填序号)原子的理论利用率为100%,符合“绿色化学”的要求。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)相对分子质量为72的烷烃,它的一氯代物只有一种,此烷烃的结构简式为 。
(2)某气态烷烃和一气态烯烃组成的混合气体在同温、同压下对氢气的相对密度为13,取标准状况下此混合气体4.48 L,通入足量的溴水,溴水质量增加2.8 g,此两种烃的组成为 (填分子式)。
(3)某烃是一种比水轻的油状液体,相对分子质量为78,碳元素与氢元素的质量比为12:1,不能使溴水和酸性高锰酸钾溶液褪色。写出此烃发生取代反应的化学方程式(任意写一个即可) 。
(4)2.3g某有机物A完全燃烧后,生成0.1 mol CO2和 2.7gH2O,测得该化合物的蒸气与空气的相对密度是1.6,已知此有机物可以发生催化氧化反应,写出此反应的化学方程式 。
(5) 有机物的结构可用“键线式”表示,如:![]() 可简写为
可简写为![]()
![]() 可简写为
可简写为 ![]() 。玫瑰的香味物质中包含苧烯,苧烯的键线式如右图,
。玫瑰的香味物质中包含苧烯,苧烯的键线式如右图,![]() ,苧烯的分子式为 。
,苧烯的分子式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸是生物体的一种代谢产物,菠菜、苋菜等植物中富含草酸,但在人体中容易与钙离子形成草酸钙导致肾结石。某化学研究小组为了研究草酸,查阅资料获取了以下信息。
① 草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易升华,易溶于水。
② 草酸晶体受热脱水,170℃以上分解产生CO、CO2和H2O。
③ 草酸为二元酸:K1=5.4×10-2,K2=5.4×10-5。
④ 草酸的钠盐和钾盐易溶于水。
(1)研究小组为了验证草酸受热分解产生的CO2,按照如下图所示的装置进行实验。装置B中可观察到的现象是 。但研究小组指导老师认为实验方案欠妥,要求改进实验。小组同学一致同意在A、B之间再加入一个实验装置C,其作用是 ,请在下图方框中画出该装置,并标明所需试剂。

(2)研究小组为了验证草酸受热分解产生的CO,按照(1)实验中的装置A、C和下图所示的部分装置(可以重复选用)进行实验。

实验装置依次连接的合理顺序为A→C→ →H→D→I。装置H反应管中盛有的物质是 。
(3)经过实验(1)和(2)证明草酸晶体受热分解产生了CO和CO2。请写出草酸晶体受热分解的化学方程式 。
(4)为了测定某草酸溶液的物质的量浓度,该小组查阅文献发现硫酸酸化的高锰酸钾溶液可以氧化草酸并放出CO2,反应的离子方程式为 。若利用已知浓度的酸性高锰酸钾标准液滴定未知浓度的草酸溶液,滴定终点判断方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年诺贝尔生理学或医学奖授予中国药学家屠呦呦以及爱尔兰科学家威廉·坎贝尔和日本科学家大村智,表彰他们在寄生虫疾病治疗研究方面取得的成就。屠呦呦先驱性地发现了青蒿素,开创了疟疾治疗新方法。右图为青蒿素,关于该物质的下列说法正确的是

A.青蒿素化学式为C15H20O5
B.在光照条件下可能发生取代反应
C.可以与氢气发生加成反应
D.水浸青蒿对治疗疟疾有良好的疗效
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5有机化学基础】
姜黄素具有抗突变和预防肿瘤的作用,其合成路线如下:

已知:
i.1 mol G最多能消耗Na、NaOH、NaHCO3的物质的量分别为3 mol、2 mol、1 mol。
ii.![]()
iii. (R1、R2、R3为烃基或氢原子) 请回答:
(R1、R2、R3为烃基或氢原子) 请回答:
(1)B→C的反应类型是 。
(2)C→D反应的化学方程式是 。
(3)E的核磁共振氢谱中有两个峰,E中含有的官能团名称是 。
E→G反应的化学方程式是 。
(4)下列有关香兰醛的叙述不正确的是 。
a.香兰醛能与NaHCO3溶液反应
b.香兰醛能与浓溴水发生取代反应
c.1 mol香兰醛最多能与3 molH2发生加成反应
(5)写出一种符合下列条件的香兰醛的同分异构体的结构简式 。
①苯环上的一硝基取代物有2种
②1 mol该物质水解,最多消耗3 molNaOH
(6)姜黄素的分子中有2个甲基,其结构简式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com