
科目:高中化学 来源: 题型:
一定温度下,下列溶液的离子浓度关系式正确的是( )。
A、pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5 mol·L—1
B、pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C、pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:
c(Na+)+ c(H+)= c(OH-)+c( HC2O4-)
D、pH相同的 ①CH3COONa ②NaHCO3 ③NaClO 三种溶液的c(Na+):①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
实验中需要2 mol·L-1的Na2CO3溶液950 mL,配制时,你认为应该选用的容量瓶的规格和称取的碳酸钠质量分别是( )。
A.1000 mL, 212 g B.950 mL, 201.4 g
C.500 mL, 286 g D.任意规格, 572 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的制备合理的是( )
①将氯化铝与硫化钾溶液混合后过滤来制备硫化铝②将过量的铁与氯气加热反应制备氯化亚铁③在配制的硫酸亚铁溶液常加入一定量的铁粉和硫酸④铜先氧化成氧化铜,再与硫酸反应来制取硫酸铜⑤将45mL冰加入到盛有5g氯化钠的烧杯中,溶解配制50g质量分数为5%的氯化钠溶液
A.只有④ B.只有②③ C.只有③④ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是从铝土矿中制备铝的工艺流程:
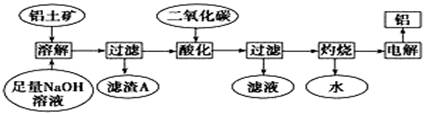
已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的Na2SiO3与Na2[Al(OH)4]与反应,能生成硅铝酸盐沉淀,化学反应方程式为:
2Na2SiO3+2Na2[Al(OH)4]=2Na2Al2Si2O8↓+2H2O+4 NaOH
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中主要发生反应的离子方程式:__________________________;_____________________________。
(2)滤渣A的主要成分为 ;滤渣A的用途是(只写一种)
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、R是1~18号元素中的四种元素,它们的原子结构有以下特点:
①元素X原子的M层比L层少3个电子;
②元素Y的2价阴离子的核外电子排布与氖原子相同;
③元素Z原子的L层比M层多5个电子;
④元素R原子的L层比K层多3个电子,其中金属性最强的是( )
A.X B.Y C.Z D.R
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z均为短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为X2-和Z-,Y+和Z-具有相同的电子层结构。下列说法正确的是
A.原子最外层电子数:X>Y>Z B.单质沸点:X>Y>Z
C.离子半径:X2->Y+>Z- D.原子序数:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,体积恒定的密闭容器中反应 A(g)+ 3B(g)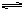 2C(g)达到平衡的标志的是( )
2C(g)达到平衡的标志的是( )
(1)C的生成速率与C的分解速率相等;
(2)单位时间内2amol C生成,同时生成3amol B;
(3)A、B、C的浓度不再变化;
(4)混合气体的总压强不再变化;
(5)混合气体的物质的量不再变化;
(6)A、B、C的分子数目比为1:3:2。
A.(2)(4)(5) B.(2)(6)
C. (1)(2)(3)(4)(5) D. (2)(5)(6)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com