
铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是从铝土矿中制备铝的工艺流程:
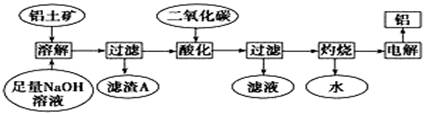
已知:(1)铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质;
(2)溶液中的Na2SiO3与Na2[Al(OH)4]与反应,能生成硅铝酸盐沉淀,化学反应方程式为:
2Na2SiO3+2Na2[Al(OH)4]=2Na2Al2Si2O8↓+2H2O+4 NaOH
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中主要发生反应的离子方程式:__________________________;_____________________________。
(2)滤渣A的主要成分为 ;滤渣A的用途是(只写一种)
科目:高中化学 来源: 题型:
常温下,水的离子积为KW,下列说法正确的是( )。
A.在pH=11的溶液中,水电离出的c(OH-)一定等于10—3mol/L
B.将pH=1的酸溶液和pH=13的碱溶液等体积混合后,混合溶液的pH一定等于7
C.将物质的量浓度和体积都相同的一元酸HA与一元碱BOH混合后,溶液呈中性,则反应后溶液中c(H+) =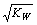
D.若强酸、强碱中和后溶液的pH=7,则中和前酸、碱的pH之和一定等于14
查看答案和解析>>
科目:高中化学 来源: 题型:
在200mL硫酸铝溶液中,含有1.5NA个硫酸根离子(NA表示阿佛加德罗常数值),同时含有NA个金属离子。则Al2(SO4)3的物质的量浓度为( )
A.2mol·L-1 B.2.5 mol·L-1 C.5 mol·L-1 D.7.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.10ml质量分数为98%的H2SO4,用10ml水稀释后,H2SO4的质量分数大于49%
B.配制0.1mol/L的Na2CO3溶液480ml,需用500ml容量瓶
C.在标况下,将22.4L氨气溶于1L水中,得到1mol/L的氨水
D.向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2和 Na2O,使溶液均恰好饱和,则加入的Na2O2 与Na2O的物质的量之比等于1:1(保持温度不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
列叙述错误的是( )
A.NH3的喷泉实验说明氨气极易溶于水
B.NO 和NH3均可用排空气法收集
C.盛液溴的瓶内加少量水可防止液溴的挥发
D.NH3遇到挥发性的强酸就能冒白烟
查看答案和解析>>
科目:高中化学 来源: 题型:
根据稳定岛假说,元素周期表的最终界限可能在175号元素左右,科学家预测114号元素位于第七周期ⅣA族,下列有关此元素的预测中,正确的是( )
A.它为非金属 B.其离子比Cu2+离子的氧化性强
C.其低价氧化物是酸性氧化物 D.它有+2价与+4价
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与平衡移动无关的是( )
A.向0.1 mol/L的CH3COOH中加水稀释,溶液pH增大
B.向氯水中投入AgNO3,最终溶液酸性增强
C.夏天,打开冰镇啤酒的盖子后,有大量的气泡冒出
D.在滴有酚酞的Na2CO3溶液中,慢慢滴入BaCl2溶液,溶液的红色逐渐褪去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com