
����Ŀ������������һ��ѪС��ۼ����Ƽ�����һ���ϳ�·�����£������Լ�����Ӧ����ʡ�ԣ���

��֪��![]()
���������գ�
��1��д����Ӧ�����Լ�����������________________��________________
��2��д����Ӧ���͡���_________________��________________
��3��д��D�Ľṹ��ʽ��___________________
��4��д��һ�ַ�������Ҫ���C��ͬ���칹��Ľṹ��ʽ��___________________
i.�ܷ���������Ӧ
ii.������-O-O-�ṹ
iii. ������ֻ���������ڶ�λ�ĺ���ȡ����
��5�����һ����A������ͬϵ��ϳɾ۱���ϩ�ĺϳ�·�ߡ�___________________
���ϳ�·�߳��õı�ʾ��ʽΪ��![]() ��
��
��6�����ݷ�Ӧ���з�Ӧ�����������뷴Ӧλ�ÿ��Եó��Ľ�����______________��
���𰸡� Cl2��Fe����FeCl3�� CH3OH��H2SO4������ ���� ȡ�� ![]()
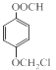 ��
��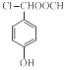 ��
��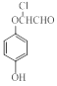 ���������ɣ�2�֣�
���������ɣ�2�֣� ![]() �뱽��ֱ��������Cl���ܵ�����Ӱ�죬���Խ��ͣ���������ȡ��
�뱽��ֱ��������Cl���ܵ�����Ӱ�죬���Խ��ͣ���������ȡ��
�����������ݷ�Ӧ��������ṹ��ʽ���ж�A�Ǽױ�������ȡ����Ӧ����B��B�Ľṹ��ʽΪ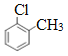 ��B����������Ӧ����ת��ȩ�������ݷ�Ӧ�����������ʽ���жϸ÷�Ӧ���Ȼ���״�����������Ӧ������D�ķ���ʽ��֪��Ӧ�����ǻ�����ԭ��ȡ������D�Ľṹ��ʽΪ
��B����������Ӧ����ת��ȩ�������ݷ�Ӧ�����������ʽ���жϸ÷�Ӧ���Ȼ���״�����������Ӧ������D�ķ���ʽ��֪��Ӧ�����ǻ�����ԭ��ȡ������D�Ľṹ��ʽΪ ��D������֪��Ϣ�ķ�Ӧ��������������
��D������֪��Ϣ�ķ�Ӧ��������������
��1���������Ϸ�����֪��Ӧ�����Լ��������ֱ��ǣ���Cl2��Fe����FeCl3������CH3OH��H2SO4�����ȣ���2���������Ϸ�����֪��Ӧ����������Ӧ������ȡ����Ӧ����3��D�Ľṹ��ʽΪ ����4��i. �ܷ���������Ӧ������ȩ����ii. ������-O-O-�ṹ��iii. ������ֻ���������ڶ�λ�ĺ���ȡ��������˷����������л���ṹ��ʽΪ
����4��i. �ܷ���������Ӧ������ȩ����ii. ������-O-O-�ṹ��iii. ������ֻ���������ڶ�λ�ĺ���ȡ��������˷����������л���ṹ��ʽΪ  ��
�� ��
�� ����5����A������ͬϵ��ϳɾ۱���ϩ������������ұ�����ϳ�·��Ϊ
����5����A������ͬϵ��ϳɾ۱���ϩ������������ұ�����ϳ�·��Ϊ![]() ����6����Ӧ�����뱽��ֱ����������ԭ��û�б�ȡ����������ǣ��뱽��ֱ��������Cl���ܵ�����Ӱ�죬���Խ��ͣ����Ա�ȡ����
����6����Ӧ�����뱽��ֱ����������ԭ��û�б�ȡ����������ǣ��뱽��ֱ��������Cl���ܵ�����Ӱ�죬���Խ��ͣ����Ա�ȡ����


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ��������������ˮ�е�ijЩ�ɷ֣����������ʣ�û�й�ϵ���ǣ� ��
A.��NaHCO3�������������ˮ�У�����ɫ���ݣ�H+��
B.ʹ��ɫ������ɫ��HCl��
C.��FeCl2��Һ�еμ���ˮ���ٵμ�KSCN��Һ�����ֳʺ�ɫ��Cl2��
D.�μ�AgNO3��Һ���ɰ�ɫ������Cl����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijҩ��H�ĺϳ�·������ͼ��ʾ���Իش��������⣺
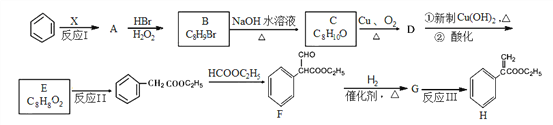
��1����Ӧ����XΪ������������������뱽��ͬ����X������______________��
��2��д�ṹ��ʽ��A__________��D_____________��
��3��д����Ӧ��ķ�Ӧ������_________________��
��4��д����Ӧ���ͣ�A��B__________��C��D__________��
��5��д��G��H�Ļ�ѧ��Ӧ����ʽ��________________________________________��
��6��д��������������������E��ͬ���칹��Ľṹ��ʽ��____________��___________��
�ٷ���������Ӧ �ڱ�������2��ȡ���� �����ڲ�ͬ�����л���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ʒ�ˮ�г����о綾��NaCN����������������������
�ٵ�һ�Σ�NaCN+NaClO��NaOCN+NaCl
�ڵڶ��Σ�NaOCN+NaClO��Na2CO3+CO2��+NaCl+N2����δ��ƽ��
���������գ�
��1��������Ӧ�漰��Ԫ���У���ԭ�Ӻ���δ�ɶԵ�������______����
O2����Na+��Cl���а뾶��С����_____________��
��2��NaCN�����к��еĻ�ѧ������Ϊ___________________��
��3���ڶ��ι����У��������ڹ��ۻ�����ĵ���ʽ��___________��������__________������ԡ��Ǽ��ԡ������ӡ�
��4����֪��NaOCN��NԪ��Ϊ-3�ۡ���ƽ�ڶ��ι��̵Ļ�ѧ����ʽ���������ת�Ƶķ������Ŀ��_______________
��5���ۺ����η�Ӧ����������0.01 mol NaCN�ķ�ˮ��������NaClO________mol��
��6������һ������ʽ֤�����ķǽ����Դ���̼��_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2CO(g)��O2(g)===2CO2(g) ��H����566 kJ��mol��1
Na2O2(s)��CO2(g)===Na2CO3(s)��![]() O2(g) ��H����226 kJ��mol��1
O2(g) ��H����226 kJ��mol��1
���������Ȼ�ѧ����ʽ�жϣ�����˵����ȷ����( )
A. CO��ȼ����Ϊ283 kJ
B. ��ͼ�ɱ�ʾ��CO����CO2�ķ�Ӧ���̺�������ϵ
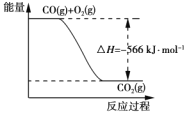
C. 2Na2O2(s)��2CO2(s)===2Na2CO3(s)��O2(g) ��H>��452 kJ��mol��1
D. CO(g)��Na2O2(s)��Ӧ�ų�509 kJ����ʱ������ת����Ϊ6.02��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ� ��
A. �����£���pH=3��CH3COOH��Һ��pH=3��H2SO4��Һ�У�ˮ�ĵ���̶�ǰ��С�ں���
B. 0.1 molL��1 CH3COONa��Һ��0.05 molL��1����������Ϻ��������Һ�У�c��Cl������c��CH3COO������c��CH3COOH����c��H+��
C. ij�¶�ʱˮ�����ӻ�����KW��10��13���������¶���pH��11��NaOH��Һa L��pH��1��ϡ����b L��ϣ������û��ҺpH��2����a��b��9 ��2��������Һ��Ϻ������仯��
D. �����£���10 mL pH��12������������Һ�м���pH��2��HA��pH�պõ���7��������Һ���V(��)��20 mL��������Һ��Ϻ������仯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�������������ֱ�ͨ����ʼ�����ͬ���ܱ������������У�ʹ�䷢����Ӧ��t0ʱ�������дﵽ��ѧƽ�⣬X��Y��Z�����ʵ����ı仯��ͼ��ʾ���������й��ƶ���ȷ���ǣ� ��
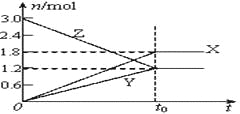
A. �÷�Ӧ�Ļ�ѧ����ʽΪ��3X+2Y![]() 2Z
2Z
B. ���������о��ﵽƽ��ʱ�������������V��������V�����������������ﵽƽ������ʱ��С��t0
C. ���������о��ﵽƽ��ʱ����������Z�����ʵ���������ͬ����YΪ��̬��Һ̬
D. ����ƽ��������������¶�ʱ�����������˵��Z�����ķ�ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��R��WΪ���ֶ�����Ԫ�ء�Xԭ�������������Ǻ�����Ӳ�����3����Y�������������۴�����Ϊ4��Z�ĵ��ʳ�����Ư��ҵ��R�Ƕ�����Ԫ���н�������ǿ��Ԫ�أ�W�������еij����������������ﳣ�����²��ϡ��ش��������⣺
(1)YԪ�ص�����______�������ڱ��е�λ�ڵ�������__________��
(2)W��Z���ʻ��ϵõ�����������__________�����ѡ����ӡ����ۡ�����������Һ�м�������NaOH��Һ����Ӧ�����ӷ���ʽΪ______��
(3)��ҵ�ϳ���W�����백����1700�淢���û���Ӧ������һ������������һ�ּ�Ӳ��ĥ�Ĺ��壬��д���÷�Ӧ�Ļ�ѧ����ʽ_________________________��
(4)���������Ԫ��X��R��ɣ�������ˮ���ҷ�Ӧ���������������ݣ�д���仯ѧ��Ӧ����ʽ______���ĵ���ʽΪ_____________��
(5)Ϊ�Ƚ�Ԫ��X��Y�ķǽ�����ǿ�������з��������е���___��
a���Ƚ�������Ԫ�صij������ʵķе�
b���Ƚ�������Ԫ�صĵ������������ϵ�����
c���Ƚ�������Ԫ�ص���̬�⻯����ȶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ç������һ�ֺϳ�����������ҩ���Ƶ�ԭ�ϣ����������ƻ������ʯ���ֲ���С����й����������л��������˵����ȷ����( )
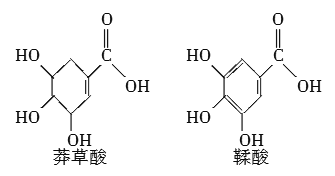
A�������ᶼ������ˮ�����ӳɷ�Ӧ
B�������������Ȼ�����Һ���ܷ�����ɫ��Ӧ
C�����������ç���������ȶ�������̼̼˫��
D�������ʵ������������������Ľ����Ʒ�Ӧ��������������ͬ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com