
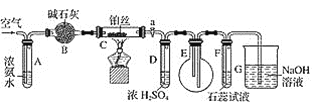
【题目】某校化学小组学生利用如图装置进行“氨的催化氧化及检验产物”实验(图中夹持装置已略去)。下列推断合理的是( )
A.C不需要持续加热
B.D的作用是干燥气体
C.B是无用装置
D.仅用该套装置和药品无法达到检验产物的目的
【答案】AD
【解析】
浓氨水易挥发,鼓入空气将挥发的浓氨水吹入B装置,B中的碱石灰用来干燥氨气,干燥的氨气在C中发生催化氧化生成一氧化氮和水,用浓硫酸吸收生成的水和剩余的氨,剩余干燥的一氧化氮在E中遇到空气发生氧化反应生成红棕色的二氧化氮,二氧化氮与F中的水生成硝酸,溶液显酸性,能够使石蕊变红色,最后用氢氧化钠溶液吸收过量的二氧化氮,据此解答。
A. 氨气的催化氧化为放热反应,放出的热量能够维持反应继续进行,铂丝不需要持续加热;故A正确;
B. 装置B的作用为干燥氨气,装置D的作用不是用来干燥气体,而是通过浓硫酸质量的变化检验水的生成,但装置D中的浓硫酸除了能够吸收水外,还能吸收未参加反应的氨气,故B错误;
C. 装置B的作用为干燥氨气,故C错误;
D. 不能通过D装置增重得出结论反应生成水,一氧化氮为无色,而一氧化氮容易被氧化为红棕色的二氧化氮,所以也不能通过颜色断定氨气的催化氧化生成的氮氧化物,故D正确;
推断合理的是AD。


科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中进行化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数和温度的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=____________。
(2)该反应为____________(填“吸热”或“放热”)反应。
(3)某温度下,平衡浓度符合下式c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____________℃。
(4)在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)=2 mol·L-1,c(H2)=1.5 mol·L-1,c(CO)=1 mol·L-1,c(H2O)=3 mol·L-1,则下一时刻,反应____________(填“正向”或“逆向”)进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲、乙、丙、丁代表4种纯净物。甲(g)+2乙(g) ![]() 丙(g)+丁(g) ΔH=-a kJ·mol1 (a>0),下列说法正确的是
丙(g)+丁(g) ΔH=-a kJ·mol1 (a>0),下列说法正确的是
A. 甲(g)的能量一定大于丙(g)的能量
B. 该反应不需要加热
C. 1 mol甲(g)与2 mol乙(g)的总能量高于1 mol丙(g)和1 mol丁(g)的总能量
D. 在一密闭容器中充入1 mol 甲(g)与2 mol 乙(g),在一定条件下反应放出的热量为a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
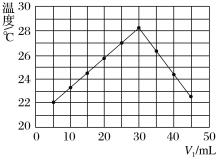
【题目】将V1mL1.00mol·L-1HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是( )
A.该实验表明化学能可以转化为热能
B.做该实验时环境温度为22℃
C.NaOH溶液的浓度约为1.00mol·L-1
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)亚硝酸钠(NaNO2)外观酷似食盐,但它是一种有毒的物质。误食亚硝酸钠会使人体血液中的Fe2+转化为Fe3+而引起中毒,服用维生素C可使Fe3+转化为Fe2+,从而达到解毒的目的。转化过程可表示为:Fe2+![]() Fe3+,转化1中,氧化剂是____,转化2中,维生素C表现____性。
Fe3+,转化1中,氧化剂是____,转化2中,维生素C表现____性。
(2)在①盐酸、②浓硝酸、③氨水、④稀硫酸、⑤氢氧化钠溶液五种物质中,可用于除去Al表面的铜镀层的是_____(填序号);实验室常用硫酸铝溶液和____(填序号)反应制取氢氧化铝,反应的离子反应方程式是_____。
(3)把一定量铜粉投入氯化铁、氯化铜的混合溶液中,完全反应后,所得溶液中Cu2+、Fe2+和Fe3+三种离子的浓度恰好相等。则原溶液中的Fe3+和Cu2+的物质的量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸镍广泛应用于电镀、催化、医药等行业中,具有很高的经济价值。一种用含镍废催化剂(主要含![]() 、C,还含有铝、铁的单质及氧化物,和少量有机物)为原料制备
、C,还含有铝、铁的单质及氧化物,和少量有机物)为原料制备![]() 的工艺流程如下:
的工艺流程如下:

部分阳离子以氢氧化物形式沉淀时的![]() 如下:
如下:
沉淀物 | 开始沉淀时的 | 完全沉淀时的 |
| 2.7 | 3.2 |
| 7.6 | 9.7 |
| 7.1 | 9.2 |
回答下列问题:
(1)滤液a中溶质的主要成分除![]() 外,还含有_________________(填化学式)。
外,还含有_________________(填化学式)。
(2)酸溶前需进行“热处理”的主要目的是____________;滤渣b主要成分是________(填化学式)。
(3)加入![]() 溶液时发生反应的离子方程式为_______;简述加入
溶液时发生反应的离子方程式为_______;简述加入![]() 除杂的原理_______。
除杂的原理_______。
(4)操作d为________、过滤、洗涤、干燥;产品晶体中有时会混有少量![]() ,其原因可能是__________。(写出一点即可)
,其原因可能是__________。(写出一点即可)
(5)取ag上述流程制得的硫酸镍晶体样品溶于蒸馏水中,在不断搅拌下缓慢加入足量丁二酮肟溶液![]() ,再加入
,再加入![]() 溶液调节溶液的
溶液调节溶液的![]() 在8~9,充分反应后,过滤、洗涤、烘干、称量得到红色固体质量为bg。发生反应的方程式为
在8~9,充分反应后,过滤、洗涤、烘干、称量得到红色固体质量为bg。发生反应的方程式为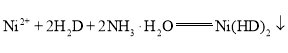 (红色)
(红色)![]() ,已知
,已知![]() 相对分子质量为M,列式计算样品纯度为_________。
相对分子质量为M,列式计算样品纯度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 用洁净的铂丝蘸取某食盐试样,在酒精灯火焰上灼烧,火焰显黄色 | 说明该食盐试样不含 |
B |
|
|
C | 向某溶液中滴加 | 溶液中含 |
D | 将石蜡油蒸气通过炽热的碎瓷片分解得到的气体通入溴的四氯化碳溶液,溴的四氯化碳溶液褪色 | 分解产物中含乙烯 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示甲、乙是电化学实验装置。
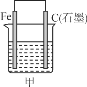
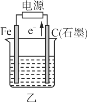
(1)若甲、乙两烧杯中均盛有NaCl溶液。
①甲中石墨棒上的电极反应式为__________________________________。
②乙中总反应的离子方程式为____________________________________。
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为_________。
(2)若甲、乙两烧杯中均盛有CuSO4溶液。
①甲中铁棒上的电极反应式为__________________________。
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25 ℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入________(填写物质的化学式)________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72-转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应堆起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验。请完成以下实验设计表(表中不要留空格)。
实验序号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
① | 4.0 | 60.0 | 10.0 | 30.0 |
② | 5.0 | 60.0 | 10.0 | 30.0 |
③ | 5.0 | 60.0 | ______ | ______ |
测得实验①和②溶液中Cr2O72-的浓度随时间变化关系如图所示。
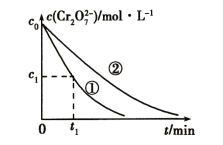
(2)上述反应的离子方程式为_______。
(3)对比实验①和②的结果可得出结论______。实验①中0~t1时间段反应速率v(Cr3+)=_____(用代数式表示)。
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如了下假设,请你完成假设二:
假设一:Fe2+起催化作用;
假设二:___________;
······
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com