


科目:高中化学 来源: 题型:
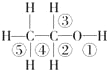
| A、和金属钠反应时键①断裂 |
| B、和氢溴酸反应时键①断裂 |
| C、和浓硫酸共热140℃时键①或键②断裂;170℃时键②⑤断裂 |
| D、在Ag催化下和O2反应键①③断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应△H>0 |
| B、强电解溶液的导电能力一定强于弱电解质溶液的导电能力 |
| C、CH3COOH、Cu(OH)2、BaSO4、NH3都是常见的弱电解质 |
| D、常温下就能发生的化学反应一定是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸易挥发,而硫酸难挥发 |
| B、常温常压下,溴呈液态,碘呈固态 |
| C、稀有气体一般很难发生化学反应 |
| D、氮气的化学性质比氧气稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
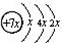 .B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
.B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
| B、IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 |
| C、Fe3O4可以写成FeO3;Pb3O4也可以写成PbO?Pb2O3 |
| D、NaHSO4与NaHSO3溶于水显酸性,由所有酸式盐溶于水显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.9 mol/L |
| B、0.64 mol/L |
| C、0.5 mol/L |
| D、0.32 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性氧化物都是非金属氧化物 |
| B、碱性氧化物都是金属氧化物 |
| C、由同种元素构成的物质一定属于纯净物 |
| D、难溶于水的电解质一定是弱电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com