
56 26 |
| A、26 | B、30 | C、56 | D、82 |
科目:高中化学 来源: 题型:
| A、酸性 HClO4<HBrO4<HIO4 |
| B、碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2 |
| C、稳定性 HCl>PH3>H2S |
| D、还原性 Cl->Br->I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有②③ | B、只有③④ |
| C、只有①③ | D、只有①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=0.5mol/(L?s) |
| B、v(B)=0.3 mol/(L?s) |
| C、v(C)=0.8 mol/(L?s) |
| D、v(D)=1 mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10种 | B、15种 |
| C、18种 | D、24种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非金属性:Si>C>P>Cl>F |
| B、热稳定性;HCl>H2S>PH3>AsH3 |
| C、酸性强弱:H3AlO3<H2SiO4<H2CO3<H3PO4 |
| D、离子半径;F->Na+>Mg2+>Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构如图所示,下列有关该化合物的说法不正确的是( )
一种从植物中提取的天然化合物αdamascone可用于制作“香水”,其结构如图所示,下列有关该化合物的说法不正确的是( )| A、分子式为C14H20O |
| B、该化合物可发生聚合反应 |
| C、1mol该化合物完全燃烧消耗17.5mol O2 |
| D、1mol该化合物能与2 mol Br2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1CH3COOH溶液加水稀释,溶液中所有离子浓度均减小 |
| B、常温下,在由水电离出的c(OH-)=1×10-12mol?L-1的溶液中,Al3+可能大量存在 |
| C、常温下,向AgCl悬浊液中加入少量NaCl固体后振荡,Ksp(AgCl)增大 |
| D、常温下,相同浓度的CH3COONa溶液与Na2CO3溶液相比,Na2CO3溶液的pH小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
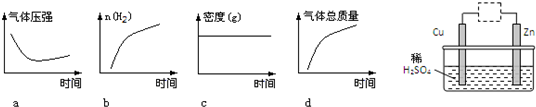
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com