
关于晶体的自范性,下列叙述正确的是( )。
| A.破损的晶体能够在固态时自动变成规则的多面体 |
| B.缺角的氯化钠晶体在饱和的NaCl溶液中慢慢变为完美的立方块 |
| C.圆形容器中结出的冰是圆形的 |
| D.由玻璃制成的圆形的玻璃球 |
科目:高中化学 来源: 题型:单选题
下列数据是对应物质的熔点: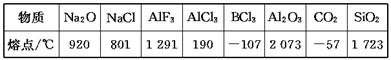
据此做出的下列判断中错误的是( )
| A.铝的化合物的晶体中有的是离子晶体 |
| B.表中只有BCl3和干冰是分子晶体 |
| C.同族元素的氧化物可形成不同类型的晶体 |
| D.不同族元素的氧化物可形成相同类型的晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
NaCl的晶胞如图所示,将NaCl晶胞中的所有Cl-去掉,并将Na+全部换成C原子,再在晶胞的4个“小立方体”中心处各放置一个C原子,且这四个“小立方体”互不共面,位于“小立方体”中的碳原子均与最近的4个碳原子成键,以此表示金刚石的一个晶胞。若再将在成键的C原子中心联线的中点处增添一个O原子,则构成了某种CO2的晶胞。则下面说法正确的是( )(已知C-C键的键长1.54×10-10m)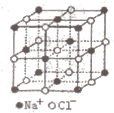
| A.一个金刚石的晶胞中有8个C原子 |
| B.金刚石的密度为3.54g·cm-1 |
| C.在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成 |
| D.在该种CO2晶胞中含氧原子8个 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某离子化合物的晶胞如右图所示立体结构,晶胞是整个晶体中最基本的重复单位。小黑球表示阳离子,小白球表示阴离子,该离子化合物中,阴、阳离子个数比是
| A.1∶8 | B.1∶4 | C.1∶2 | D.1∶1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
决定物质性质的重要因素是物质结构。请回答下列问题。
(1)下图是石墨的结构,其晶体中存在的作用力有 (填序号) 
A:σ键 B:π键 C:氢键 D:配位键 E:分子间作用力 F:金属键 G:离子键
(2) 下面关于晶体的说法不正确的是___________
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4 |
| B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.熔点由高到低:Na>Mg>Al |
| D.晶格能由大到小:NaF> NaCl> NaBr>NaI |


查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列对化学知识概括合理的是( )。
| A.原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键 |
| B.同素异形体之间的转化都是物理变化 |
| C.原子晶体的熔点不一定比金属晶体的高,分子晶体的熔点不一定比金属晶体的低 |
| D.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
关于金属晶体的体心立方密堆积的结构型式的叙述中,正确的是( )。
| A.晶胞是六棱柱 |
| B.属于A2型密堆积 |
| C.每个晶胞中含有4个原子 |
| D.每个晶胞中含有5个原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列数据是对应物质的熔点(℃):
| BCl3 | Al2O3 | Na2O | NaCl | AlF3 | AlCl3 | 干冰 | SiO2 |
| -107 | 2 073 | 920 | 801 | 1 291 | 190 | -57 | 1 723 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述不正确的是( )
| A.金刚石、碳化硅、晶体硅的熔点依次降低 |
| B.CaO晶体结构与NaCl晶体结构相似,每个CaO晶胞中含有4个Ca2+和4个O2- |
C.设NaCl的摩尔质量为M g·mol-1,NaCl的密度为ρ g·cm-3,阿伏加德罗常数为NA mol-1,在NaCl晶体中,两个距离最近的Cl-中心间的距离为 · · cm cm |
| D.X、Y可形成立方晶体结构的化合物,其晶胞中X占据所有棱的中心,Y位于顶角位置,则该晶体的组成式为XY3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com