
【题目】已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:
H2O2→H2O IO3-→I2 MnO4-→Mn2+ HNO2→NO
如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
A.H2O2 B.IO3-
C.MnO4- D.HNO2
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】电解质的水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。
① 醋酸在水溶液中的电离方程式为 。
② 下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是 (填字母序号)。
a.滴加少量浓盐酸 b.微热溶液
c.加水稀释 d.加入少量醋酸钠晶体
(2)用0.1 mol·L-1 NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 mol·L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
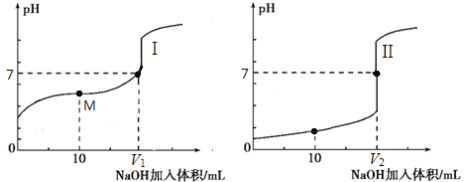
滴定醋酸的曲线是 (填“I”或“II”)。
② 滴定开始前,三种溶液中由水电离出的c(H+)最大的是 。
③ V1和V2的关系:V1 V2(填“>”、“=”或“<”)。
④ M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 。
(3)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度:AgSCN > AgI。
操作步骤 | 现象 |
步骤1:向2 mL 0.005 mol·L-1 AgNO3溶液中加入2 mL 0.005 mol·L-1 KSCN溶液,静置。 | 出现白色沉淀。 |
步骤2:取1 mL上层清液于试管中,滴加1滴2 mol·L-1 Fe(NO3)3溶液。 | 溶液变红色。 |
步骤3:向步骤2的溶液中,继续加入5滴3 mol·L-1 AgNO3溶液。 | 现象a ,溶液红色变浅。 |
步骤4:向步骤1余下的浊液中加入5滴3 mol·L-1 KI溶液。 | 出现黄色沉淀。 |
写出步骤2中溶液变红色的离子方程式 。
步骤3中现象a是 。
用化学平衡原理解释步骤4的实验现象 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将纯水加热至较高温度,下列叙述正确的是( )
A. 水的离子积变大,pH变小,呈酸性
B. 水的离子积不变,pH不变,呈中性
C. 水的离子积变小,pH变大,呈碱性
D. 水的离子积变大,pH变小,呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】类比推理是化学中常用的思维方法。下列推理正确的是( )

A.HCl可以用如图装置完成喷泉实验, 推测HF可以用此装置完成喷泉实验
B.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3
C.SiH4的沸点高于CH4,推测H2Se的沸点高于H2S
D.NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化硼(BCl3)是一种重要的化工原料,可用于制取乙硼烷(B2H6),也可作有机合成催化剂。某兴趣小组拟选用下列装置制备BCl3(已知BCl3的沸点为12.5 ℃,熔点为-107.3 ℃;2B+6HCl![]() 2BCl3↑+3H2↑。
2BCl3↑+3H2↑。

请回答下列问题:
(1)装置B中发生反应的化学方程式为 。
(2)按气流方向连接各装置的接口,顺序为a-( )- ( )- ( )- ( )- ( )-( )-f-g-h。连接好装置后的实验操作是__________________________。
(3)装置D的作用是 ;实验中若不用装置C,可能产生的危险是 。
(4)BCl3遇水发生水解观察到大量的白雾,生成两种酸,其反应的化学方程式为:_____________。
(5)装置E的作用除了可以吸收多余Cl2外,还起到的作用是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为10L的密闭容器中,进行如下反应:A(g)+2B(g)![]() C(g)+D(g),最初加入1.0mol A和2.2mol B,在不同温度下,D的物质的量n(D)和时间t的关系如图1.
C(g)+D(g),最初加入1.0mol A和2.2mol B,在不同温度下,D的物质的量n(D)和时间t的关系如图1.

试回答下列问题:
(1)800℃时,0~5min内,以B表示的平均反应速率为 .
(2)能判断反应达到化学平衡状态的依据是 (填字母).
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3)若最初加入1.0mol A和2.2mol B,利用图中数据计算800℃时的平衡常数K=__________,该反应为__________反应(填“吸热”或“放热”).
(4)700℃时,某时刻测得体系中物质的量浓度如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol,n(D)=0.9mol,则此时该反应__________(填“向正方向进行”、“向逆方向进行”或“处于平衡状态”).
(5)在催化剂作用下,CO可用于合成甲醇:CO(g)+2H2(g)CH3OH(g)若在恒温恒压的条件下,向密闭容器中充入4mol CO和8mol H2,合成甲醇,平衡时CO的转化率与温度、压强的关系如图所示:

①该反应的正反应属于__________反应;(填“吸热”或“放热”).
②在0.1Mpa、100℃的条件下,该反应达到平衡时容器内气体的物质的量为 mol。
若在恒温恒容的条件下,向上述平衡体系中充入4mol CO,8mol H2,与原平衡状态相比,达到平衡时CO转化率 (填“增大”,“不变”或“减小”),平衡常数K (填“增大”,“不变”或“减小”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是( )
A.加入少量水,水的电离平衡向正反应方向移动
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.再通入少量氯气,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图Ⅰ是NO2(g)+CO(g)![]() CO2(g)+NO(g)反应过程中能量变化示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态.当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ,下列有关说法正确的是
CO2(g)+NO(g)反应过程中能量变化示意图.一定条件下,在固定容积的密闭容器中该反应达到平衡状态.当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ,下列有关说法正确的是

A.一定条件下,向密闭容器中加入1molNO2(g)与1molCO(g)反应放出234 kJ热量
B.若X表示CO的起始浓度,则Y表示的可能是NO2的转化率
C.若X表示反应时间,则Y表示的可能是混合气体的密度
D.若X表示温度则Y表示的可能是CO2物质的量浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com