
【题目】填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:________.
(2)周期表中最活泼的非金属元素位于第________纵行.
(3)A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两种元素的原子核外电子数之和等于B原子的质子数,
![]()
请回答下列问题:写出A、B两种元素的符号:A________,B________.B在周期表中位置是 ________________.
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】诺贝尔物理学奖曾授予“光纤之父”英国华裔科学家高锟以及两位美国科学家威拉德·博伊尔和乔治·史密斯。光导纤维的主要成分是二氧化硅,下列关于二氧化硅的说法正确的是( )
A. 二氧化硅是酸性氧化物,因此能与水反应生成硅酸
B. 用二氧化硅制取单质硅时,当生成2.24 L气体(标准状况)时,得到2.8 g硅
C. 二氧化硅制成的光导纤维,由于导电能力强而被用于制造光缆
D. 二氧化硅不能与碳酸钠溶液反应,但能与碳酸钠固体在高温时发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢(H2O2)在医药、化工、民用等方面有广泛的应用。回答下面问题:
(1)最早制备H2O2使用的原料是易溶于水的BaO2和稀硫酸,发生反应的化学方程式是____。
(2)目前工业制备H2O2的主要方法是蒽醌法。反应流程如下:
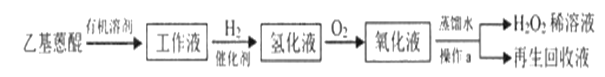
已知:乙基蒽醌是反应中的催化剂。
①蒽醌法所用原料的物质的量之比为____。
②操作a是____。
③再生回收液的成分是____。
(3)测量过氧化氢浓度常用的方法是滴定法,某次测定时,取20. 00mL过氧化氢样品,加入过量硫酸酸化,用0. l000mol/L的KMnO4标准溶液滴定至终点,消耗10. 00mL,滴定时发生反应的离子方程式为 ___,该样品中H2O2的物质的量浓度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于卤化氢的说法中不正确的是( )
A. 卤素原子序数越大,其氢化物越稳定
B. 卤素原子序数越大,其氢化物越不稳定
C. 卤化氢稳定性的顺序为HF>HCl>HBr>HI
D. 卤素单质与氢气越难反应,生成的氢化物越不稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图所示(部分反应条件及产物略去)。
![]()
(1)若A是一种黄色单质固体,则B→C的化学方程式为_____________________。浓的D溶液使纸张变黑体现了它的___________性。
(2)若C是红棕色气体,则A化学式可能____________;试写出C生成D的化学方程式____________________________________________________;写出稀的D溶液与铜反应的离子方程式____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.SiO2溶于水且显酸性
B.SiO2是制造太阳能电池的常用材料
C.SiO2是酸性氧化物,它不与任何酸反应
D.水玻璃可用作木材防火剂,向其溶液中通入CO2气体,有白色凝胶状固体析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiAlH4( )、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是
A. LiH与D2O反应,所得氢气的摩尔质量为4 g/mol
B. 1 mol LiAlH4在125℃完全分解,转移3 mol电子
C. LiAlH4溶于适量水得到无色溶液,则化学方程式可表示为:LiAlH4+ 2H2O![]() LiAlO2+ 4H2↑
LiAlO2+ 4H2↑
D. LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中不正确的是( )
A. 0.1 mol·L-1 NH4HS溶液中有:c(NH![]() )<c(HS-)+c(S2-)+c(H2S)
)<c(HS-)+c(S2-)+c(H2S)
B. 25 ℃时,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合后,c(NH![]() )=c(Cl-),则NH3·H2O的电离常数为
)=c(Cl-),则NH3·H2O的电离常数为![]()
C. 等浓度的HCN和NaCN混合溶液中有:2c(Na+)=c(CN-)+c(HCN)
D. 等pH的HA和HB溶液,分别与一定浓度的氢氧化钠溶液完全中和,HA消耗的氢氧化钠溶液体积多,则可证明酸性HA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】瑞典化学家舍勒将软锰矿(主要成分为MnO2)与浓盐酸混合加热,在世界上首先制得了氯气。如图是某研究性学习小组设计制取氯气并以氯气为反应物进行特定反应的装置。
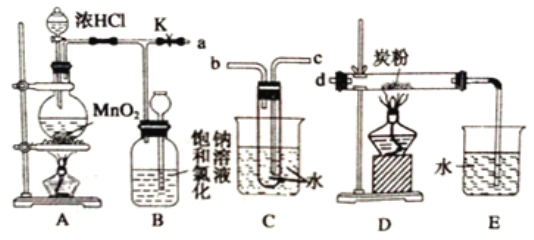
(1)A中制取Cl2反应的化学方程式是_________。
(2)要将C装置接入B和D之间,正确的接法是a→________→_____________→d。
(3)实验开始先点燃A处的酒精灯,打开夹子K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为________。为了使C装置发挥更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com