
已知33As、35Br位于同一周期,下列关系正确的是
A 原子半径:As>C1>P B 热稳定性:HC1>AsH3>HBr
C 还原性:As3->S2->C1- D 酸性:H3AsO4>H2SO4>H3PO4
科目:高中化学 来源: 题型:单选题
短周期元素R、T、Q、W、G在元素周期表中的相对位置如图所示,其中Q是无机非金属材料的主角。下列判断正确的是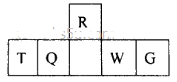
| A.离子半径:T< W<G |
| B.等物质的量的W、G单质分别与足量铁粉反应,后者消耗的铁粉多 |
| C.最简单气态氢化物的热稳定性:Q<R |
| D.T和G组成的化合物溶于水,其水溶液呈中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图是元素周期表的一部分,下列说法正确的是( )
| A.可在灰色区域“甲”中寻找催化剂 |
| B.离子半径:W-﹥Y3-﹥X+ |
| C.气态氢化物的稳定性:Z﹥W |
| D.工业上电解X和W化合物的水溶液制备X |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
第三周期元素,浓度均为0.01 mol/L的最高价氧化物对应水化物的pH与原子半径的关系如图所示。则下列说法正确的是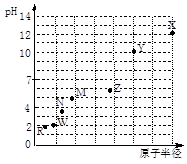
| A.气态氢化物的稳定性:N>R |
| B.Z的最高价氧化物对应的水化物能溶于稀氨水 |
| C.Y和R形成的化合物既含离子键又含共价键 |
| D.X和M两者最高价氧化物对应的水化物反应后溶液的pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z关系如图,X原子的电子层数为n,最外层电子数为2n。W原子最内层电子数是最外层电子数的2倍。下列说法错误的是
| X | | | |
| | | Y | Z |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A.质子数:c>d | B.离子的还原性:Y2->Z- |
| C.氢化物的稳定性:H2Y>HZ | D.原子半径:X<W |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是
A 元素原子的最外层电子数等于元素的最高化合价
B 多电子原子中,在离核较近的区域内运动的电子能量较高
C P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强
D 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是
| 元素 代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | -1 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com