
【题目】某课外小组利用废旧铝铜合金(含有少量杂质铁)制备Al(OH)3,流程如下:

回答下列问题:
(1)铝铜合金很坚硬,轻而抗张强度大,可代替昂贵的铜线为电线。但该合金暴露在空气中易被腐蚀,原因是___________________________。
(2)废旧铝铜用过量的稀硫酸浸取时,发生反应的化学方程式为________________。
(3)能溶解滤渣A而不产生空气污染的方法是___________________。
(4)在温度为358~368K时,加入Al2O3调节pH=1.6~1.8,析出黄铁矾[Na2Fe6(SO4)4(OH)12]。写出析出黄铁矾的离子方程式
(5)加NH3·H2O后将沉淀经过滤、_________、_________称量,得Al(OH)3质量为废旧铝铜合金质量的2.6 倍,则废旧铝铜合金含中Al的质量分数≤________%。
(6)Al(OH)3是塑料和有机聚合物的一种理想的阻燃剂填充料。塑料或聚合物与外部热源接触而燃烧时,可分为以下几个阶段:①加热,②分解,③起火,④燃烧,⑤蔓延。Al(OH)3阻燃起作用的阶段是____________。
【答案】 铝铜合金在潮湿空气中易形成原电池,发生电化学腐蚀 2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑ 将滤渣A放入稀硫酸中,加热并不断通入O2 2Na+ + 6Fe3+ + 4SO42- + 12H2O = Na2Fe6(SO4)4(OH)12↓+12 H+ 洗涤、干燥 90% ①②
【解析】(1)铝铜合金很坚硬,轻而抗张强度大,可代替昂贵的铜线为电线。但该合金暴露在空气中,表面吸附空气中水蒸气会构成原电池,发生电化学腐蚀,故答案为:铝铜合金在潮湿空气中易形成原电池,发生电化学腐蚀;
(2)废旧铝铜用过量的稀硫酸浸取时,铝被稀硫酸溶解放出氢气,发生反应的化学方程式为2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑,故答案为:2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑;
(3)根据流程图,滤渣A中含有铜,将铜溶解而不产生空气污染的方法可以是将滤渣A放入稀硫酸中,加热并不断通入O2,铜与氧气在硫酸溶液中反应生成硫酸铜和水,故答案为:将滤渣A放入稀硫酸中,加热并不断通入O2;
(4)在温度为358~368K时,加入Al2O3调节pH=1.6~1.8,析出黄铁矾[Na2Fe6(SO4)4(OH)12]。反应的黄铁矾的离子方程式为2Na+ + 6Fe3+ + 4SO42- + 12H2O = Na2Fe6(SO4)4(OH)12↓+12 H+,故答案为:2Na+ + 6Fe3+ + 4SO42- + 12H2O = Na2Fe6(SO4)4(OH)12↓+12 H+;
(5)氧化铝被酸溶解,因此滤液B中含有铝离子有部分来自于氧化铝的溶解,加NH3·H2O后生成氢氧化铝沉淀,将沉淀经过滤、洗涤、干燥称量,得Al(OH)3质量为废旧铝铜合金质量的2.6 倍。设生成的氢氧化铝的物质的量为1mol,则废旧铝铜合金质量为![]() =
=![]() g,含有铝元素的质量为
g,含有铝元素的质量为![]() ×78g=27g,则废旧铝铜合金含中Al的质量分数≤
×78g=27g,则废旧铝铜合金含中Al的质量分数≤![]() ×100%=90%,故答案为:洗涤、干燥;90;
×100%=90%,故答案为:洗涤、干燥;90;
(6)Al(OH)3是塑料和有机聚合物的一种理想的阻燃剂填充料。Al(OH)3受热分解,吸收大量热量,使环境温度下降;同时生成的耐高温、稳定性好的Al2O3覆盖在可燃物表面,阻燃效果更佳。阻燃起作用的阶段是加热和分解阶段,故选①②。


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】实验室用下列方法测定某水样中O2的含量。
(1)实验原理。
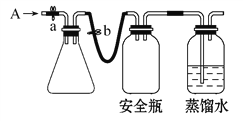
①用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为____________________________。
②在酸性条件下,再用I-将生成的MnO(OH)2还原为Mn2+,反应的离子方程式为____________________。然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为I2+2Na2S2O32NaI+Na2S4O6。
(2)实验步骤。
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是_________;
②用注射器抽取某水样20.00 mL从A处注入锥形瓶;
③再分别从A处注入含mmol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及一定浓度的硫酸(含H2SO4nmol);
⑥重复④的操作;
⑦取下锥形瓶,向其中加入2~3滴__________作指示剂;
⑧用0.005 mol·L-1Na2S2O3溶液滴定至终点。滴定终点的现象是_____________。
(3)数据分析。
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为________mg·L-1。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将__________(填“偏大”“偏小”或“不变”)。
③实验要求加入适量的H2SO4使溶液接近中性,其原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数,下列叙述正确的是( )
A.标准状况下,22.4 L H2O含有的分子数为1 NA
B.常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下,1 NA 个CO2分子占有的体积为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl﹣ 个数为1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12。
(1)该温度下,水的离子积常数Kw=________________。
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=_________,此时该溶液中由水电离的c(OH-)=____________。
(3)该温度下,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2是我国大部分地区雾霾天气产生的主要原因之一。加大SO2的处理力度,是治理环境污染的当务之急。SO2主要来自于汽车尾气、燃煤烟气、硫酸工业尾气、冶金工业烟气等。
(1)“催化转换器”能将汽车尾气中CO与NO转化成可参与大气生态环境循环的无毒气体,并促进烃类充分燃烧及SO2的转化,但也在一定程度上提高了空气的酸度。“催化转换器”提高空气酸度的原因是_____________________________。
(2)用氨水将燃煤烟气中的SO2转化成NH4HSO3。该法是利用了SO2________(填选项字母编号)
A.漂白性 B.氧化性 C.还原性 D.酸性氧化物性质
(3)用生物质热解气(主要成分CO、CH4、H2)将燃煤烟气中SO2在高温下还原成单质硫。主要发生了下列反应:
2H2(g) +SO2(g)= S(g) + 2H2O(g) △H1 = + 90.4kJmol-1
2CO(g) +O2(g)= 2CO2(g) △H2 = - 566.0kJmol-1
S(g) +O2(g)= SO2(g) △H3 = - 574.0kJmol-1
试写出CO将SO2还原成S(g)的热化学方程式__________________________。
(4)将硫酸工业尾气中的SO2转化成硫酸,同时获得电能。装置如图所示(电极均为惰性材料):
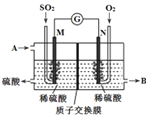
①溶液中的H+移向_______。(填“M”或“N”)
②M极发生的电极反应式为________________。
③写出A、B所代表的物质的化学式:
A_______、B ________。
(5)利用硫酸钠溶液吸收冶金工业烟气中SO2,再用惰性电极电解,能获得所需的产品,装置如图所示。
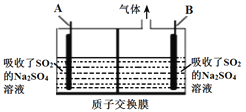
①若电解后A极区得到硫酸,则B电极反应式为________________________。
②若电解后A极区析出硫磺,则电解反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】80 ℃时,2 L 密闭容器中充入0.40 mol N2O4,发生反应N2O4![]() 2NO2 △H =+Q kJ/mol(Q>0),获得如下数据:下列判断正确的是
2NO2 △H =+Q kJ/mol(Q>0),获得如下数据:下列判断正确的是
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
A. 升高温度该反应的平衡常数K减小
B. 20~40 s 内,v(N2O4)=0.002 mol/( Ls)
C. 反应达平衡时,吸收的热量为0.30 Q kJ/mol
D. 100s 时再通入0.40 mol N2O4,达新平衡时N2O4的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列式子正确且属于水解反应,溶液又呈碱性的是
A. HCO3-+H2O![]() H3O++CO32- B. Fe3++3H2O
H3O++CO32- B. Fe3++3H2O![]() Fe(OH)3+3H+
Fe(OH)3+3H+
C. HS-+H2O![]() H2S+OH- D. CO32-+H2O
H2S+OH- D. CO32-+H2O![]() H2CO3+OH-
H2CO3+OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物是大气污染物之一,消除氮氧化物的方法有多种。
Ⅰ催化还原法
(1)利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160 kJ/mol
则CH4将NO2还原为N2的热化学方程式为____________________________。
(2)利用NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。反应的化学方程式为:2NH3(g)+NO(g)+NO2(g)![]() 2N2(g)+3H2O(g) ΔH < 0。为提高氮氧化物的转化率可采取的措施是_______________(写出1条即可)。
2N2(g)+3H2O(g) ΔH < 0。为提高氮氧化物的转化率可采取的措施是_______________(写出1条即可)。
(3)在汽车排气管内安装的催化转化器,可使尾气中主要污染物转化为无毒物质。主要反应如下:2NO(g)+ 2CO(g)![]() N2(g)+ 2CO2(g)。在一定温度下,向体积为1L的密闭容器中通入2molNO、1molCO,发生上述反应,10分钟时反应达到平衡状态,此时容器中CO变为0.6molL-1。
N2(g)+ 2CO2(g)。在一定温度下,向体积为1L的密闭容器中通入2molNO、1molCO,发生上述反应,10分钟时反应达到平衡状态,此时容器中CO变为0.6molL-1。
①前10分钟内用氮气表示的反应速率为___________,计算该温度下反应的平衡常数K为______Lmol-1。(只列算式,不要求计算结果)
②若保持温度不变,在15分钟时向容器内再次充入NO 1.6 mol、CO2 0.4 mol,则此时反应的ν正___ν逆(填“<”、“=”或“> ”)
II 氧化法。
(4)首先利用ClO2 氧化氮氧化物,再利用还原剂还原为无毒的氮气。其转化流程如下:
NO![]() NO2
NO2![]() N2。
N2。
已知反应Ⅰ的化学方程式为2NO+ ClO2 + H2O =NO2 + HNO3 + HCl,则反应Ⅱ的化学方程式是_____________________________;若生成11.2 L N2(标准状况),则消耗ClO2____________g 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com