
����Ŀ������ȼ�ϵ�������л���Ϊȼ�ϣ�ֱ�ӻ�������ø��Ϊ������һ�������ȼ�ϵ�أ�������ת���ʸߣ���һ�����������ϵ���ɫ��أ��乤��ԭ����ͼ��ʾ����֪C1���ĵ缫��ӦΪC2H5OH��3H2O��12e��=2CO2��12H��������˵���в���ȷ����(����)
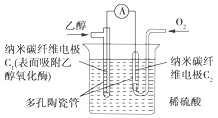
A.C1��Ϊ��ظ�����C2��Ϊ�������
B.C2���ĵ缫��ӦΪO2��4H����4e��=2H2O
C.������ȼ�ϵ�ص��ܷ�Ӧ����ʽΪC2H5OH��3O2=2CO2��3H2O
D.������C2�������·����C1��
���𰸡�D
��������
����ɿ�֪װ��Ϊȼ�ϵ�أ��Ҵ�Ϊȼ�ϣ�����Ϊ�����������ܷ�ӦΪC2H5OH��3O2=2CO2��3H2O��C1��ͨ���Ҵ���Ϊȼ�ϵ�صĸ�����C1��ͨ�����������Ϊȼ�ϵ�ص��������ɴ��жϡ�
����ɿ�֪װ��Ϊȼ�ϵ�أ��Ҵ�Ϊȼ�ϣ�����Ϊ�����������ܷ�ӦΪC2H5OH��3O2=2CO2��3H2O��C1��ͨ���Ҵ���Ϊȼ�ϵ�صĸ�����C2��ͨ�����������Ϊȼ�ϵ�ص����������ܷ�Ӧ��C1���ĵ缫��Ӧ�ɵ�C2���ĵ缫��ӦΪ��O2��4H����4e��=2H2O��
A. �ɷ�����֪��C1��ͨ���Ҵ���Ϊȼ�ϵ�صĸ�����C2��ͨ�����������Ϊȼ�ϵ�ص�������A����ȷ��
B. ���ܷ�Ӧ��C1���ĵ缫��Ӧ�ɵ�C2���ĵ缫��ӦΪ��O2��4H����4e��=2H2O��B����ȷ��
C. ȼ�ϵ�����Ҵ�Ϊȼ�ϣ�����Ϊ�����������ܷ�ӦΪC2H5OH��3O2=2CO2��3H2O��C����ȷ��
D.ԭ����е����ɸ����������ƶ�������C1�������·����C2����D�����
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ԫ��������Ҫ�Ľ���Ԫ��֮һ���䲻���Ǹ��ֲָĵ���Ҫ�ɷ֣��ܶຬ��������Ҳ������Ҫ���塣
��1�����յ����Ų����ɰ�Ԫ�����ڱ��е�Ԫ�ػ��ֳ����������Ԫ������____����
��2��Fe-Cr-Al�Ͻ����Ϊ����β�����������壬����β�������ɽ�NO2��ԭΪ���������壬��ֹHNO3��������γɣ�NO2�Ŀռ乹��Ϊ____��HNO3������ǿ��HNO2��ԭ��Ϊ___��
��3����������������ԭ�Ӳ������������ѻ�����������Ŀռ�������Ϊ___���ú�����ʽ�ӱ�ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ͽ�1molCl2(g)�еĻ�ѧ����Ҫ����242.7kJ�����������ݷ�ӦH2(g)��Cl2(g)=2HCl(g)�������仯ʾ��ͼ������˵������ȷ���ǣ� ��
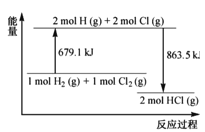
A.H2(g)��Cl2(g)=2HCl(g) ��H=-184.4kJ��mol-1
B.HCl(g)=![]() H2(g)��
H2(g)��![]() Cl2(g) ��H=92.2kJ��mol-1
Cl2(g) ��H=92.2kJ��mol-1
C.�Ͽ�1molH2(g)�еĻ�ѧ����Ҫ����436.4kJ������
D.H2(g)��Cl2(g)�γ�1molHCl(g)�ͷ�863.5kJ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڳ�����pH=12�İ�ˮ��������������Һ������˵����ȷ����
A.��ˮ��Һ��Ũ�ȴ�������������Һ
B.NH3��H2O�ĵ��뷽��ʽ��NH3��H2O��NH4+��OH��
C.c(NH3��H2O)��c(NH4+)��0.01mol��L��1
D.������Һϡ��100������ϡ�ͺ���Һ��pHֵ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() ͭ�ۺ�þ�۵Ļ����ֳ�2�ȷݣ�������һ�ݼ���200mL��ϡ�����в����ȣ����������ǡ����ȫ��Ӧ����������״���µ�NO
ͭ�ۺ�þ�۵Ļ����ֳ�2�ȷݣ�������һ�ݼ���200mL��ϡ�����в����ȣ����������ǡ����ȫ��Ӧ����������״���µ�NO![]() ������һ���ڿ����г�ּ��ȣ����õ�mg���壮�����й�˵����
������һ���ڿ����г�ּ��ȣ����õ�mg���壮�����й�˵����![]() ��
��![]() �����������Ũ�ȣ�
�����������Ũ�ȣ�![]() ��
��![]() ��������ȷ����
��������ȷ����
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���2 L���ܱ������з�����Ӧ��xA��g����B��g��![]() 2C��g������H��0��A��C�����ʵ�����ʱ��仯�Ĺ�ϵ���±���ʾ�������й�˵����ȷ���ǣ�������
2C��g������H��0��A��C�����ʵ�����ʱ��仯�Ĺ�ϵ���±���ʾ�������й�˵����ȷ���ǣ�������
ʱ��/min | n��A��/mol | n��C��/mol |
0 | 0.3 | 0 |
1 | 0.15 | 0.15 |
2 | 0.1 | 0.2 |
3 | 0.1 | 0.2 |
A.x��1
B.��Ӧ��ʼ2 min�ڣ���B��ʾ�ķ�Ӧ����Ϊ0.05 mol��L��1��min��1
C.��Ӧ���е�1 minʱ����Ӧ��ϵ�ﵽ��ѧƽ��״̬
D.A������Ӧ���ʵ���C���淴Ӧ����ʱ����Ӧ��ϵ�ﵽ��ѧƽ��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��̽������ȼ�ϵ�ع���ԭ����װ��ʾ��ͼ��ʵ��ʱ���ȱպ�S1���Ͽ�S2�����ˮһ��ʱ����ٶϿ�S1���պ� S2���������ܳ������⡣�ٶϿ�S1�պ� S2ʱ�������й�˵����ȷ���ǣ�������
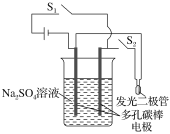
A.�����̼���缫����������ʧȥ���ӣ�������ԭ��Ӧ
B.�Ҳ���̼���缫���������缫��ӦʽΪ��O2��2H2O��4e��=4OH��
C.����ת����ʽΪ����������ѧ��������
D.Na���������̼��Ǩ�ƣ������ɸ��������·��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ͼ���˵����ȷ����

A. ͼ�ױ�ʾ����ij������Һ����μ���NaOH��Һ�����������ɳ��������ʵ�����μ�NaOH��Һ����Ĺ�ϵ
B. ͼ�ұ�ʾ�������ʵ�����NaOH��Na2CO3�Ļ����Һ����μ���ϡ��������������������������μ�HCl��Һ����Ĺ�ϵ
C. ͼ����ʾ����ϡ������Һ��������������������Һ��Fe3�����ʵ����������������ʵ����ı仯��ϵ
D. ��ȥ������������������Ȼ��ƿ��á�����Ũ�������ȹ��ˡ��ķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ijЩ�������ȡ���ռ���β������װ����ͼ��ʾ��ʡ�Լгֺ;���װ�ã������ô�װ�úͱ����ṩ������������ʵ�飬�������ѡ����

ѡ�� | a�е����� | b�е����� | c���ռ������� | d�е����� |
A | Ũ��ˮ | CaO | NH3 | H2O |
B | Ũ���� | Na2SO3 | SO2 | NaOH��Һ |
C | ϡ���� | Cu | NO2 | H2O |
D | Ũ���� | MnO2 | Cl2 | NaOH��Һ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com