
【题目】将![]() 铜粉和镁粉的混合物分成2等份,将其中一份加入200mL的稀硝酸中并加热,固体和硝酸恰好完全反应,并产生标准状况下的NO
铜粉和镁粉的混合物分成2等份,将其中一份加入200mL的稀硝酸中并加热,固体和硝酸恰好完全反应,并产生标准状况下的NO![]() ;将另一份在空气中充分加热,最后得到mg固体.下列有关说法:
;将另一份在空气中充分加热,最后得到mg固体.下列有关说法:![]() ;
;![]() 无法计算硝酸的浓度;
无法计算硝酸的浓度;![]() ;
;![]() ,其中正确的是
,其中正确的是
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是
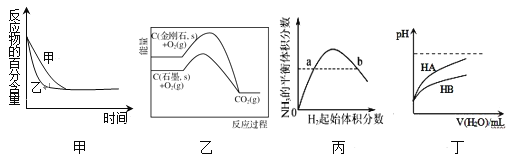
A.图甲表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
B.图乙是金刚石与石墨分别氧化生成CO2的能量关系曲线,说明石墨转化为金刚石的反应的ΔH>0
C.图丙表示一定条件下的合成氨反应中,NH3的平衡体积分数随H2起始体积分数(N2的起始量恒定)的变化,图中a点N2的转化率大于b点
D.图丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予三位对锂电池研究作出杰出贡献的科学家。一种锂-空气电池如图所示。当电池工作时,![]() 与
与![]() 在多孔碳材料电极处生成
在多孔碳材料电极处生成![]() (
(![]() 或1)。下列说法正确的是
或1)。下列说法正确的是
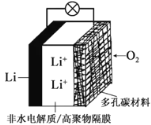
A.锂电极发生氧化反应
B.多孔碳材料电极为负极
C.电池工作时外电路电子由多孔碳材料电极流向锂电极
D.正极的电极反应式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可用甲苯合成苯甲醛:
 ,
,
下列说法正确的是
A. 甲苯分子中所有原子都在同一平面内 B. 反应①②③的反应类型相同
C. 一氯甲苯的同分异构体有3种 D. 苯甲醇可与金属钠反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
①已知:放电时,负极的电极反应式为Zn-2e-+2OH-=Zn(OH)2,则正极反应式为__。
②放电时,_____(填“正”或“负”)极附近溶液的碱性增强。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
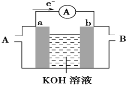
①使用时,空气从_____口通入(填“A”或“B”);
②假设使用的“燃料”是甲醇(CH3OH),a极的电极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生物燃料电池是以有机物为燃料,直接或间接利用酶作为催化剂的一类特殊的燃料电池,其能量转化率高,是一种真正意义上的绿色电池,其工作原理如图所示。已知C1极的电极反应为C2H5OH+3H2O-12e-=2CO2+12H+。下列说法中不正确的是( )
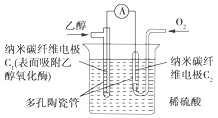
A.C1极为电池负极,C2极为电池正极
B.C2极的电极反应为O2+4H++4e-=2H2O
C.该生物燃料电池的总反应方程式为C2H5OH+3O2=2CO2+3H2O
D.电子由C2极经外电路流向C1极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Z所处的族序数是周期序数的2倍。下列判断正确的是
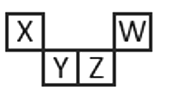
A.最高正化合价:X<Y<Z<W
B.原子半径:W<X<Y<Z
C.气态氢化物的热稳定性:Z<W
D.最高价氧化物对应水化物的酸性:Z<W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸是二元弱酸,0.2 mol·L-1NaHC2O4溶液显酸性,关于NaHC2O4溶液中离子浓度关系的叙述不正确的是( )
A.c(Na+)>c(HC2O4—)>c(C2O42—)>c(H2C2O4)
B.c(Na+)=c(HC2O4—)+c(C2O42—)+c(H2C2O4)
C.c(Na+)+c(H+)=c(HC2O4—)+c(C2O42—)+c(OH-)
D.c(H+)+c(H2C2O4)=c(C2O42—)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeOCr2O3,还含有二氧化硅、氧化铝等杂质。制备流程如图所示:
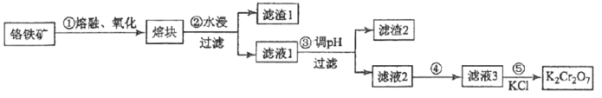
(1)步骤①的主要反应为:FeOCr2O3+NaOH+O2![]() Na2CrO4+Fe2O3+H2O 。
Na2CrO4+Fe2O3+H2O 。
上述反应配平后氧化剂与还原剂的系数比为__________。
若在实验室中进行步骤①,应该在_______中进行(填序号)
A.石英坩埚 B.铁制坩埚 C.氧化铝坩埚 D.陶瓷坩埚
(2)滤渣1中含量最多的金属元素是__________(填元素符号);滤渣2的主要成分是_________及含硅杂质;步骤③调滤液1的pH使之变_________(填“大”或“小”)
(3)向“滤液3”中加入适量KCl,经结晶过滤得到K2Cr2O7固体。步骤⑤的反应类型是___________反应。
(4)某工厂用380 kg 铬铁矿粉(含Cr2O3 40%)制备K2Cr2O7,最终得到产品250 kg,产率为________×100%(保留2位有效数字,M(Cr2O3)=152g/mol;M(K2Cr2O7)=294g/mol)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com