
【题目】某学习小组为研究电化学原理,设计如图装置.下列叙述不正确的是( ) 
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e﹣=Cu
C.a和b分别连接足够电压的直流电源正、负极时,Cu2+向铜电极移动
D.无论a和b是否用导线连接,铁片均溶解,溶液从蓝色逐渐变成浅绿色
【答案】C
【解析】解:A.a和b不连接时,发生Fe+Cu2+=Cu+Fe2+置换反应,则铁片上会有金属铜析出,故A正确;
B.a和b用导线连接时,Cu为正极,在正极上阳离子得电子,则发生Cu2++2e﹣=Cu,故B正确;
C.a和b分别连接足够电压的直流电源正、负极时,形成电解池,b与负极相连为阴极,阳离子向阴极移动,所以Cu2+向Fe电极移动,故C错误;
D.无论a和b是否用导线连接,均发生Fe+Cu2+=Cu+Fe2+,则铁片均溶解,溶液从蓝色逐渐变成浅绿色,故D正确;
故选C.
A.a和b不连接时,发生置换反应;
B.a和b用导线连接时,Cu为正极,在正极上阳离子得电子;
C.a和b分别连接足够电压的直流电源正、负极时,形成电解池,b为阴极,阳离子向阴极移动;
D.无论a和b是否用导线连接,均发生Fe+Cu2+=Cu+Fe2+.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素。如图转化关系中所涉及的物质含有这五种元素的单质或化合物,其中反应①是置换反应,A为金属单质,D为非金属单质,原子核外最外层电子数D是A的2倍,F是一种最高价含氧酸,遇光或热会分解。下列说法正确的是
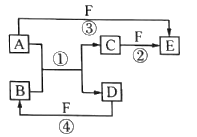
A. 简单氢化物的沸点:Z>W
B. Y与W形成的化合物都可以和氢氧化钠溶液反应
C. Y、Z、W元素中,原子半径最小的是W
D. W与Q组成的常见化合物中可能含有极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaBH4燃料电池具有理论电压高、能量密度大等优点。已知,能量密度=电池输出电能/燃料质量,以该燃料电池为电源电解精炼铜的装置如图所示。下列说法不正确的是
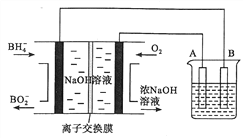
A. 离子交换膜应为阳离子交换膜,Na+由左极室向右极室迁移
B. 该燃料电池的负极反应式为BH4-+8OH--8e-=B![]() +6H2O
+6H2O
C. 若NaBH4 燃料电池的电压为U伏,则此电池的能量密度为2.03×104UkJ·kg-1
D. 每消耗2.24 L O2(标准状况)时,A电极的质量减轻12.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,判断下列叙述中正确的是( ) 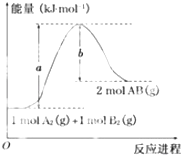
A.每生成2分子AB吸收b kJ热量
B.断裂1mol A﹣A和1mol B﹣B键,放出a kJ能量
C.该反应中反应物的总能量高于生成物的总能量
D.该反应热△H=+(a﹣b)kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家研制出合成药物W对肝癌的治疗,具有很好的效果。其由有机物A合成药物W的合成路线如下:
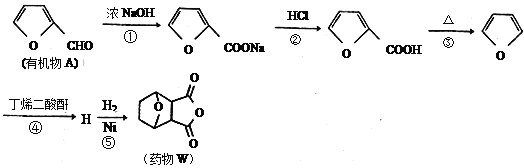
已知:①2HCHO+NaOH→CH3OH+HCOONa
②![]() (Diels-Aider反应)
(Diels-Aider反应)
③丁烯二酸酐结构简式为![]()
④当每个1,3-丁二烯分子与一分子氯气发生加成反应时,有两种产物:
CH2ClCH=CHCH2Cl;CH2ClCHClCH=CH2。
请回答下列问题:
(1)物质A中的含氧官能团名称为_______;第①步反应中除生成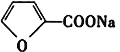 外,还生成另一产物,此产物的结构简式为__________________。
外,还生成另一产物,此产物的结构简式为__________________。
(2)写出H的结构简式_____________;第⑤步反应的反应类型是____________。
(3)药物W与N互为同分异构体。
①能与FeCl3溶液发生显色反应 ②能与Na2CO3溶液反应生成气体
③1mol N能与3mol NaOH完全反应
写出满足上述条件且其核磁共振氢谱有4个吸收峰的N的一种结构简式(不考虑立体异构)_____________________。
(4)下面是合成X的路线图:
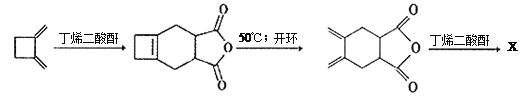
则X的结构简式为___________________。
(5)结合题中有关信息,写出由![]() 制备丁烯二酸酐
制备丁烯二酸酐![]() 的合成路线流程图______________(无机试剂任选)。合成路线流程图示例如下:
的合成路线流程图______________(无机试剂任选)。合成路线流程图示例如下:
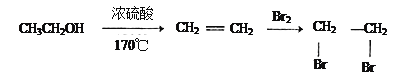 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )
A.Mg的摩尔质量是24g/mol
B.22gCO2物质的量为2.2mol
C.1molCl2中含有的氯原子数约为6.02×1023
D.常温常压下,1molN2的体积是22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiCIO4。溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。

回答下列问题:
(1)外电路的电流方向是由____极流向____极。(填字母)
(2)电池正极反应式为__ __。
(3)是否可用水代替电池中的混合有机溶剂?____(填“是”或“否”),原因是_________ ___。
(4)MnO2可与KOH和KClO3,在高温下反应,生成K2MnO4,反应的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+3B(g) =2C(g)+2D(g)在四种不同情况下的反应速率分别为:①v(A)=0.45 mol·L-1·s-1、②v(B)=0.6 mol·L-1·s-1、③v(C)=0.4 mol·L-1·s-1、④v(D)=0.45 mol·L-1·s-1,该反应进行的快慢顺序为
A. ①>③=②>④ B. ①>②=③>④
C. ②>①=④>③ D. ①>④>②=③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴化亚铜可用于彩色照相,是一种白色结晶状粉末,见光分解,在空气中会慢慢氧化成绿色,溶于氢溴酸、盐酸、硝酸和氨水,在热水中也会发生分解。实验室制备CuBr的装置示意图和步骤如下:
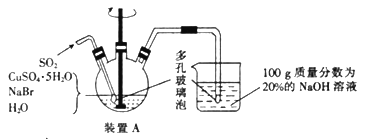
实验步骤:
①在装置A中加人50.0 g CuSO4o5H2O、30.9 g NaBr、150 mL蒸馏水,60℃时不断搅拌,以适当流速通入SO2;
②溶液冷却后倾去上层清液,在避光的条件下过滤;
③依次用溶有少量SO2的水、溶有少量SO2的乙醇、纯乙醚洗涤;
④在双层干燥器(分别装有浓硫酸和氢氧化钠)中干燥34h,再经氢气流干燥,最后进行真空干燥,得到产品21.6 g。
回答下列问题:
(1)步骤②中过滤需要避光的原因是________________________________________________。
(2)步骤①中实验所用蒸馏水事先要进行的处理操作是_______________,控制反应在60℃条件下进行,实验中可采取的措施是________________________。
(3)步骤③中洗涤剂需“溶有SO2”的原因是__________________________________;最后洗涤剂改用乙醚的目的是_____________________________________。
(4)装置A中反应生成CuBr的离子方程式为__________________________;说明反应已完成的现象是_____________________________________________________。
(5)本实验产品的产率是_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com