
| 电离能/KJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
| 5+3 |
| 2 |


科目:高中化学 来源: 题型:
| A、某特定反应的平衡常数仅是温度的函数 |
| B、催化剂不能改变平衡常数的大小 |
| C、平衡常数发生变化,化学平衡不一定发生移动 |
| D、化学平衡发生移动,平衡常数不一定发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1L0.1mol?L-1的氨水中含有的NH3?H2O分子数为0.1NA |
| B、2.3 g金属钠与过量的氧气反应,无论加热与否转移电子数均为0.1NA |
| C、惰性电极电解食盐水,若线路中通过1 NA电子,则阳极产生气体11.2L |
| D、电解精炼铜时,若阳极质量减少6.4g,则电路中转移电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示装置进行试验((图中铁架台仪器均已略去),在Ⅰ中加入试剂后,塞紧 橡皮塞,立即打开止水夹,Ⅱ中有气泡冒出,一段时间后关闭止水夹,Ⅱ中液面上升,溶液由无色变为浑浊.符合以上试验现象的Ⅰ和Ⅱ中应加入的试剂是( )
如图所示装置进行试验((图中铁架台仪器均已略去),在Ⅰ中加入试剂后,塞紧 橡皮塞,立即打开止水夹,Ⅱ中有气泡冒出,一段时间后关闭止水夹,Ⅱ中液面上升,溶液由无色变为浑浊.符合以上试验现象的Ⅰ和Ⅱ中应加入的试剂是( )| A | B | C | D | |
| Ⅰ | CaCO3、稀HCl | Na2CO3、稀H2SO4 | Zn稀H2SO4 | Cu、稀H2SO4 |
| Ⅱ | KNO3 | NaCl | BaCl2 | Ba(OH)2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
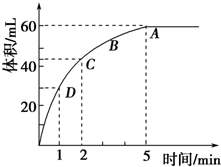 为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2 粉末于 50mL密度为1.1g?cm-3 的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如右图所示.请依图回答下列问题:
为了研究MnO2与双氧水(H2O2)的反应速率,某学生加入少许的MnO2 粉末于 50mL密度为1.1g?cm-3 的双氧水溶液中,通过实验测定:在标准状况下放出气体的体积和时间的关系如右图所示.请依图回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A原子的最外层电子数比B原子的最外层电子数少 |
| B、A的氢氧化物为两性化合物,B的氢氧化物为碱 |
| C、A元素的电负性比B元素的电负性小 |
| D、1摩尔A从酸中置换出H+生成的氢气比1摩尔B从酸中置换的H+生成的氢气多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com